Οι μέχρι σήμερα
Η χημική ένωση του
μήνα
[Ιούνιος
2008]
Επιμέλεια σελίδας:
Θανάσης Βαλαβανίδης, Καθηγητής
-
Κωνσταντίνος
Ευσταθίου, Καθηγητής
|
Φυσικoχημικές ιδιότητες:
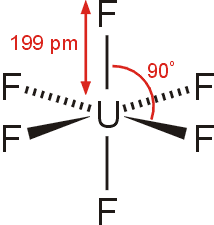
Εμφάνιση: Πτητικό, λευκό κρυσταλλικό
(μονοκλινές) στερεό.
Μοριακός τύπος: UF6
Σχετική μοριακή μάζα:
352,02
Σχετική πυκνότητα : 5,09
(= d420,7 ως στερεό), 3,595 (= d470 ως
υγρό)
Σημείο τήξης:
64,8ºC
Θερμοκρασία εξάχνωσης:
56,5ºC
Κρίσιμη θερμοκρασία: 230,2ºC, κρίσιμη πίεση: 45,5 atm
Τάση ατμών στους 25ºC: 115 mm Hg
Διαλυτότητα: αντιδρά με το νερό
(υδρολύεται προς UO2F2 και
HF), ενώ διαλύεται σε υγρό χλώριο και βρώμιο.
Ακόμη διαλύεται στο νιτροβενζόλιο και σε χλωριωμένους διαλύτες
(CCl4, CHCl3, CHCl2CHCl2). Τα διαλύματα αυτά δεν είναι σταθερά.
Σταθερά διαλύματα παρέχει σε υπερφθοριωμένους υδρογονάνθρακες (π.χ.
υπερφθοροκλυκλοεξάνιο, υπερφθοροεπτάνιο)
Γεωμετρία μορίου: Κανονικό οκτάεδρο
(δεδομένα από την
Αναφ. 1) |
 |
|
Εξαφθοριούχο
ουράνιο
Uranium
Hexafluoride
|
Μορφή στην οποία πρέπει να μετατραπεί το φυσικό ουράνιο για να
εμπλουτισθεί σε ισότοπο U-235 (πυρηνικό καύσιμο).
Οι τεράστιες ποσότητες του
"απεμπλουτισμένου" και επομένως άχρηστου UF6 που απομένουν, δημιουργούν έντονο
πρόβλημα διάθεσης και αποθήκευσης.
 |
 |
|
Martin
Klaproth (1743-1817). Γερμανός χημικός. Ανακάλυψε τα στοιχεία
ουράνιο και ζιρκόνιο.
|
Eugène-Melchior Péligot
(1811-1890). Γάλλος αναλυτικός χημικός που πρώτος παρασκεύασε μεταλλικό
ουράνιο. |
Ιστορικό της ανακάλυψης του ουρανίου και της σύνθεσης του εξαφθοριούχου ουρανίου
Το μεταλλικό
στοιχείο ουράνιο ανακαλύφθηκε
το 1789 από τον Γερμανό χημικό
Martin Klaproth,
στο ορυκτό πισουρανίτη (pitchblende),
μια ποικιλία του ορυκτού ουρανινίτης (κυρίως UO2,
με μικρές ποσότητες UO3) με πισσώδη
εμφάνιση (pitch: πίσσα),
που βρέθηκε
στα ορυχεία
αργύρου Joachimsthal
της Βοημίας (σημερινή Τσεχία). Να σημειωθεί ότι από τον πισουρανίτη αυτού του
ορυχείου η Μαρία Κιουρί απομόνωσε το 1902 το ράδιο, που αποτελεί προϊόν της
ραδιενεργού διάσπασης του ουρανίου.
Το μεταλλικό ουράνιο
απομονώθηκε πολύ αργότερα, το 1841,
από τον Eugène-Melchior Péligot, ο
οποίος το παρασκεύασε με αντίδραση άνυδρου UCl4
με μεταλλικό κάλιο [Αναφ. 2].
Η φυσική αφθονία του ουρανίου
στο φλοιό της γης (2,4 ppm) ξεπερνάει την αφθονία
άλλων πιο κοινών στοιχείων όπως π.χ. των As (1,5 ppm), Cd
(0,11 ppm),
Ag
(0,07 ppm),
Hg
(0,05 ppm) και Bi
(0,048 ppm).
Bρίσκεται σχεδόν παντού, όπως π.χ. σε κοινά πετρώματα και γρανίτες συχνά σε συγκεντρώσεις αρκετών ppm.
Ωστόσο, είναι σχετικά σπάνιες οι περιπτώσεις που
το ουράνιο βρίσκεται σε μεγάλες
περιεκτικότητες και ποσότητες σε ορυκτά (υπάρχουν δεκάδες ορυκτά ουρανίου, αλλά όλα θεωρούνται
σπάνια), ώστε τα αντίστοιχα κοιτάσματα να είναι οικονομικώς εκμεταλλεύσιμα.
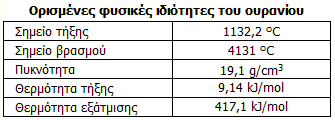 Ορισμένες
από τις φυσικές ιδιότητες του ουρανίου δίνονται στον παραπλεύρως πίνακα. Από
χημική άποψη το ουράνιο είναι χημικώς δραστικό στοιχείο με πιο σταθερές οξειδωτικές
καταστάσεις τις +4 και +6. Σε λεπτό διαμερισμό (π.χ. ως σκόνη) αντιδρά αργά με το νερό με έκλυση
υδρογόνου και είναι πυροφόρο, δηλ. μπορεί να αναφλεγεί αυτόματα οξειδούμενο από
το οξυγόνο του αέρα (π.χ. κατά τη μηχανουργική επεξεργασία). Σε συμπαγή μορφή το ουράνιο οξειδώνεται αργά στον αέρα και καλύπτεται από ένα μαύρο στρώμα
οξειδίων.
Ορισμένες
από τις φυσικές ιδιότητες του ουρανίου δίνονται στον παραπλεύρως πίνακα. Από
χημική άποψη το ουράνιο είναι χημικώς δραστικό στοιχείο με πιο σταθερές οξειδωτικές
καταστάσεις τις +4 και +6. Σε λεπτό διαμερισμό (π.χ. ως σκόνη) αντιδρά αργά με το νερό με έκλυση
υδρογόνου και είναι πυροφόρο, δηλ. μπορεί να αναφλεγεί αυτόματα οξειδούμενο από
το οξυγόνο του αέρα (π.χ. κατά τη μηχανουργική επεξεργασία). Σε συμπαγή μορφή το ουράνιο οξειδώνεται αργά στον αέρα και καλύπτεται από ένα μαύρο στρώμα
οξειδίων.
Αρχικά, λόγω της σπανιότητας του ουρανίου και της
δύσκολης
παρασκευής του σε μεταλλική μορφή, το ουράνιο ως μέταλλο δεν βρήκε καμία πρακτική εφαρμογή
παρά τις καλές μηχανικές του ιδιότητες. Οι ενώσεις του
βρήκαν από νωρίς κάποιες εφαρμογές και χρησιμοποιήθηκαν κυρίως για τον χρωματισμό υάλινων και πορσελάνινων
αντικειμένων, στα οποία προσδίδουν ένα χαρακτηριστικά φθορίζον κιτρινοπράσινο
έως μπλε χρώμα.
Ο φθορισμός των ουρανιούχων υάλων είναι ιδιαίτερα εμφανής όταν φωτιστούν με υπεριώδη ακτινοβολία.
Κάπως παράδοξο είναι το γεγονός ότι κίτρινη ύαλος με 1% οξείδιο του ουρανίου χρονολογούμενη από το 79 π.Χ. βρέθηκε στην περιοχή της Νεάπολης [Αναφ. 3].
Η ανακάλυψη της ραδιενεργού
διάσπασης του ουρανίου από τους
Otto Hahn
και Fritz Strassman
το 1938
είχε ως αποτέλεσμα ένα ουσιαστικά άχρηστο μεταλλικό στοιχείο να καταστεί το σημαντικότερο
και πλέον περιζήτητο σήμερα πυρηνικό
καύσιμο.
|

(α) |

(β) |

(γ) |

(δ) |
|
(α) Δείγμα ορυκτού ουρανινίτη
(κυρίως UO2),
το πιο κοινό ορυκτό ουρανίου (50-85% σε U3O8),
χαρακτηρίζεται από ένα ασυνήθιστα για ορυκτό μεγάλο ειδικό βάρος (8-10,5
g/cm3) [Αναφ. 4].
(β) Κρύσταλλοι του ορυκτού
καρνοτίτης K2(UO2)2(VO4)2·1-3H2O.
(γ) Αντικείμενο από ουρανιούχο
ύαλο φωτιζόμενο με υπεριώδη ακτινοβολία. (δ) Δίσκος από μεταλλικό ουράνιο με εμφανή κάλυψη σε ορισμένα
σημεία από στρώμα μαύρου οξειδίου. |
 Ισοτοπική σύνθεση και ραδιενέργεια φυσικού
ουρανίου
Ισοτοπική σύνθεση και ραδιενέργεια φυσικού
ουρανίου
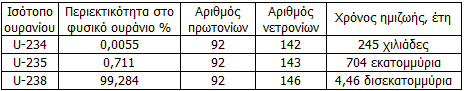
Το φυσικό ουράνιο αποτελείται από τρία ισότοπα, όλα
α-ραδιενεργά (διασπώνται εκπέμποντας σωματίδια α, δηλαδή πυρήνες He-4). Η
ισοτοπική σύνθεση του φυσικού ουρανίου και ο χρόνος ημιζωής κάθε ισοτόπου
δίνονται στον παραπλεύρως πίνακα.
Τα περισσότερο ραδιενεργά ισότοπα είναι τα U-234 και U-235 (μικρότεροι χρόνοι ημιζωής)
και
των οποίων η % περιεκτικότητα είναι πολύ μικρή. Συνεπώς, η ραδιενέργεια του
φυσικού ουρανίου είναι ασθενής και δεδομένου ότι όλα τα ισότοπα εκπέμπουν τα λιγότερο διεισδυτικά σωματίδια α (αποκόπτονται από λίγα εκατοστά
αέρα ή ένα λεπτό φύλλο χαρτιού), το ουράνιο και οι ενώσεις του γίνονται επικίνδυνα μόνο σε περίπτωση που
θα εισέλθουν στον οργανισμό μέσω του πεπτικού
ή αναπνευστικού συστήματος. Ωστόσο, τα προϊόντα
διάσπασης των ισοτόπων του ουρανίου είναι επίσης ραδιενεργά και εκπέμπουν την πλέον επικίνδυνη ακτινοβολία γ
και επομένως απαιτούνται ιδιαίτερες προφυλάξεις σε περιπτώσεις εργαζόμενων
καθημερινώς σε χώρους, όπου φυλάσσονται μεγάλες ποσότητες ουρανίου ή
ενώσεών του. 'Ετσι, μπορούμε να πούμε ότι το ουράνιο γίνεται κατά την παραμονή
του ακόμη πιο ραδιενεργό! Στοιχειώδης προφύλαξη αποτελεί ο καλός αερισμός των χώρων, ώστε
να αποφευχθεί συσσώρευση του ραδιενεργού αερίου ραδονίου (Rn),
ενός από τα θυγατρικά στοιχεία διάσπασης του U-238.
Παρά τη ραδιενέργεια του ουρανίου, αμεσότερος και μεγαλύτερος θα μπορούσε να θεωρηθεί ο κίνδυνος από τη χημική
τοξικότητα των ενώσεών του, οι χειρισμοί των οποίων πρέπει να ιδιαίτερα
προσεκτικοί, όπως ακριβώς επιβάλλεται για τις ενώσεις των τοξικών βαρέων
μετάλλων [Αναφ. 5].
Εμπλουτισμός ουρανίου και εξαφθοριούχο ουράνιο
 Το χρήσιμο (ως πυρηνικό καύσιμο) ισότοπο του
ουρανίου είναι το U-235. 'Οταν οι πυρήνες του U-235 βομβαρδιστούν με τα ονομαζόμενα "αργά" ή "θερμικά"
νετρόνια, υφίστανται σχάση (fission) με έκλυση μεγάλων ποσών ενέργειας κυρίως υπό τη
μορφή θερμότητας. Η γενική αντίδραση έχει τη μορφή:
Το χρήσιμο (ως πυρηνικό καύσιμο) ισότοπο του
ουρανίου είναι το U-235. 'Οταν οι πυρήνες του U-235 βομβαρδιστούν με τα ονομαζόμενα "αργά" ή "θερμικά"
νετρόνια, υφίστανται σχάση (fission) με έκλυση μεγάλων ποσών ενέργειας κυρίως υπό τη
μορφή θερμότητας. Η γενική αντίδραση έχει τη μορφή:
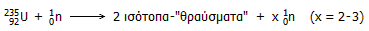
Παραπλεύρως δείχνονται τυπικές πυρηνικές
αντιδράσεις σχάσης του U-235. Περισσότερες λεπτομέρειες πάνω στη φυσική της
σχάσης του U-235
μπορούν να βρεθούν σε πολλές ιστοσελίδες του διαδικτύου
[Αναφ. 6].
Η περιεκτικότητα του φυσικού ουρανίου σε
U-235 είναι μικρή (0,7%) και δεν επαρκεί για τη συντήρηση της πυρηνικής αντίδρασης,
για την οποία απαιτείται περιεκτικότητα U-235 στα επίπεδα του 3-5%, για πυρηνικά καύσιμα πυρηνικών σταθμών παραγωγής
ενέργειας. Για την κατασκευή πυρηνικών όπλων απαιτείται ουράνιο με
περιεκτικότητα σε U-235 τουλάχιστον 20% και ιδανικά 90%
[Αναφ. 7].
Η παραγωγή του εμπλουτισμένου ουρανίου
(enriched uranium), δηλ. ουρανίου με πολύ μεγαλύτερη περιεκτικότητα σε U-235, απαιτεί ισοτοπικό
διαχωρισμό που πραγματοποιείται με μια ποικιλία τεχνικών. Οι κυριότερες από τις
τεχνικές αυτές είναι η
φυγοκέντρηση αερίου και η αέρια διάχυση. Για τις τεχνικές αυτές απαιτείται η παρασκευή
μιας πτητικής ένωσης του
ουρανίου και η μόνη πτητική ένωση του ουρανίου, που παραμένει στην αέρια φάση σε
σχετικά χαμηλές θερμοκρασίες και μπορεί να παρασκευασθεί εύκολα σε βιομηχανική κλίμακα, είναι το
εξαφθοριούχο ουράνιο (UF6).
'Ενα επιπλέον σημαντικό
πλεονέκτημα του UF6
είναι το ότι το φυσικό φθόριο αποτελείται από ένα
και μόνο ισότοπο (το F-19)
και επομένως η μοριακή
μάζα του
UF6
για το U-235 και το U-238
θα είναι αντιστοίχως 235 + 6x19 = 349
και 238 + 6x19 =
352, χωρίς την ύπαρξη άλλων συνδυασμών ατομικών μαζών, που θα προέκυπταν εάν το
φυσικό φθόριο διέθετε και άλλα σταθερά ισότοπα. Το U-234
δεν λαμβάνεται υπόψη λόγω της πολύ μικρής περιεκτικότητάς του στο φυσικό
ουράνιο.
Αυτή η διαφορά του μόλις 0,85%
στη μοριακή μάζα των εξαφθοριούχων ενώσεων του ουρανίου (θα συμβολίζονται ως 235-UF6
και 238-UF6)
είναι επαρκής για να επιτευχθεί ο απαιτούμενος
εμπλουτισμός. Ωστόσο, η
διαφορά αυτή είναι μικρή και απαιτείται μεγάλος αριθμός κύκλων διαχωρισμού, που
καθιστά την όλη διαδικασία εξαιρετικά ενεργοβόρα και φυσικά τόσο περισσότερο, όσο μεγαλύτερος είναι ο απαιτούμενος βαθμός εμπλουτισμού.
|
(α) |

(β) |

(γ) |
|
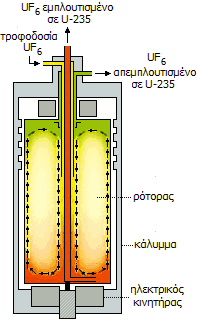
(α) Αρχή λειτουργίας φυγοκεντρικών
διαχωριστήρων. (β) Συστοιχία εκατοντάδων διαχωριστήρων για την παραγωγή
εμπλουτισμένου ουρανίου με φυγοκέντρηση αερίου. (γ)
Εργοστάσιο εμπλουτισμού ουρανίου με τη μέθοδο της αέριας διάχυσης,
στην Paducah (Κεντάκι, Ηνωμένες Πολιτείες). |
Η
φυγοκέντρηση αερίου (gas centrifugation)
βασίζεται στην ταχύτατη (50.000-70.000 rpm) περιστροφή κατακόρυφων κυλίνδρων με αέριο UF6.
Για μείωση της κατανάλωσης ενέργειας η περιστροφή τους πραγματοποιείται σχεδόν
χωρίς τριβές (σε θάλαμο κενού και με μαγνητική ανάρτηση-εναιώρηση των κυλίνδρων).
Υπό την επίδραση της φυγοκέντρου δύναμης τα βαρύτερα μόρια 238-UF6
έχουν κατά τι μεγαλύτερη τάση να κινηθούν προς τα τοιχώματα του κυλίνδρου-ρότορα
σε σχέση με τα ελαφρύτερα μόρια 235-UF6. Υπό
την επίδραση διαφοράς θερμοκρασίας μεταξύ των χαμηλότερων και υψηλότερων
τοιχωμάτων του περιστρεφόμενου κυλίνδρου δημιουργείται μια συνεχής ροή του UF6
και το εμπλουτισμένο UF6
σωρεύεται στο κάτω μέρος του κυλίνδρου, ενώ το απεμπλουτισμένο
σωρεύεται στο επάνω μέρος, απ'
όπου και συλλέγεται.
|

Αρχή λειτουργίας
εμπλουτισμού ουρανίου με την τεχνικής της αέριας διάχυσης. |
Ο βαθμός εμπλουτισμού από ένα
μόνο κύλινδρο-ρότορα είναι ελάχιστος και
για τον λόγο αυτό σε ένα εργοστάσιο εμπλουτισμού του ουρανίου υπάρχουν
συστοιχίες εκατοντάδων φυγοκεντρικών διαχωριστήρων συνδεμένων μεταξύ τους έτσι,
ώστε το εξερχόμενο και ελαφρά εμπλουτισμένο UF6
του ενός να τροφοδοτεί τον επόμενο διαχωριστήρα. Τα συστήματα αυτά απαιτούν υψηλή
τεχνολογία, αφού μια βλάβη σε ένα και μόνο κύλινδρο θα διακόψει τη συνολική
λειτουργία μιας συστοιχίας διαχωριστήρων. Αναφέρεται χαρακτηριστικά ότι υπάρχουν
συστοιχίες που λειτουργούν για δέκα χρόνια χωρίς να
χρειαστούν συντήρηση.
Η αέρια διάχυση (gaseous
diffusion)
βασίζεται στο ότι σε ένα κλειστό δοχείο όλα
τα μόρια του μίγματος
238-UF6 και 235-UF6
έχουν την ίδια ενέργεια και επομένως κατά μέσον όρο τα μόρια
235-UF6
κινούνται κατά τι ταχύτερα από τα μόρια
238-UF6
. Συνεπώς τα μόρια
235-UF6
προσκρούουν στα τοιχώματα του δοχείου λίγο πιο
συχνά απ' όσο τα μόρια
238-UF6.
Εάν μέρος των τοιχωμάτων διαθέτει μικρές οπές μεγέθους αρκετού για να διέλθουν
τα μόρια του αερίου UF6 (π.χ.
ένα πορώδες διάφραγμα), τότε μεγαλύτερο ποσοστό μορίων
235-UF6
θα διέλθει από τις οπές αυτές παρά από τα μόρια
238-UF6.
Επομένως, το εξερχόμενο UF6
είναι κατά τι πλουσιότερο σε
235-UF6,
ενώ το UF6
που παραμένει στο εσωτερικό του δοχείου είναι κατά τι φτωχότερο
235-UF6.
Μετά από 1000 στάδια επαναλαμβανόμενης διάχυσης η περιεκτικότητα του
UF6
σε 235-UF6
από 0,7% φθάνει στο 3 έως 4%.
Ο εμπλουτισμός μέσω αέριας διάχυσης είναι η μόνη τεχνική διαχωρισμού που
χρησιμοποιείται στις ΗΠΑ, ωστόσο η τεχνική αυτή είναι
κατά πολύ περισσότερο ενεργοβόρα σε σχέση με τη μέθοδο φυγοκέντρησης αερίου UF6, η οποία προβλέπεται ότι
θα είναι η τεχνική που θα επικρατήσει στο μέλλον
[Αναφ. 3β,γ].
Μονάδες έργου διαχωρισμού (SWU)
Η παραγωγική ικανότητα των
εργοστασίων εμπλουτισμού ουρανίου μετρείται σε
μονάδες έργου διαχωρισμού (separative work units,
SWU). Η μονάδα SWU είναι μια σύνθετη συνάρτηση της
ποσότητας του επεξεργαζόμενου ουρανίου και του βαθμού
εμπλουτισμού, δηλαδή μέχρι πιο ποσοστό θα πρέπει να
φθάσει η περιεκτικότητα σε U-235 στο εμπλουτισμένο
ουράνιο, σε σχέση με την παραμένουσα στο ουράνιο που
απομένει. Αποτελεί μέτρο του έργου που καταναλίσκεται
για τον εμπλουτισμό δεδομένης ποσότητας ουρανίου σε
δεδομένο ποσοστό.
Για παράδειγμα: Για να
παραχθεί 1 kg εμπλουτισμένου ουρανίου με 3% U-235 απαιτούνται: (α) 3,8 SWU, εάν το ουράνιο που
απομένει περιέχει 0,25% U-235, ή (β) 5,0 SWU αν το
ουράνιο που απομένει περιέχει 0,15% U-235. Στην
περίπτωση (α) θα χρειαστούν 6,0 kg φυσικού ουρανίου, ενώ
στη (β) μόνο 5,1 kg. Δηλαδή, όσο
περισσότερο "στραγγίζεται" το φυσικό ουράνιο από το
U-235, τόσο λιγότερη ποσότητα από αυτό χρειάζεται, αλλά
και τόσο περισσότερη κατανάλωση ενέργειας απαιτείται.
Για την τροφοδοσία με
εμπλουτισμένο ουράνιο ενός πυρηνικού εργoστασίου
ηλεκτρικής ενέργειας, με ετήσια παραγωγική ικανότητα
1000 MWe (megawatt electricity), απαιτείται έργο
διαχωρισμού 100.000 - 120.000 SWU. 'Ενα εργοστάσιο
εμπλουτισμού ουρανίου με αέρια διάχυση για 1 SWU
καταναλίσκει ενέργεια περίπου 2500 kWh, ενώ ένα σύγχρονο
εργοστάσιο εμπλουτισμού με φυγοκέντρηση αερίου
καταναλίσκει μόνο 50 kWh
[Αναφ. 3δ].
|
Βιομηχανική
παρασκευή εξαφθοριούχου ουρανίου
 Στα ορυχεία ουρανίου το μετάλλευμα του ουρανίου (με περιεκτικότητες
που μπορεί να καλύπτουν την περιοχή από 0,1 έως και 20% σε
U3O8) επεξεργάζεται συνήθως επιτόπου
με σκοπό την παρασκευή μιας εμπορικής μορφής ουρανιούχου συμπυκνώματος (concentrate), το
οποίο λόγω χρώματος και υφής είναι γνωστό ως κίτρινο κέικ (yellow cake).
Το κίτρινο κέικ τυπικά μπορεί να περιέχει 65% έως 85%
U3O8.
To U3O8
είναι μικτό οξείδιο (U3O8
= UO2·2UO3)
και αποτελεί τον συνήθη "τρόπο έκφρασης" της περιεκτικότητας σε ουράνιο
οποιουδήποτε μεταλλεύματός του (% U3O8).
Το κίτρινο κέικ αποτελεί τη μορφή με την οποία το ουράνιο αποστέλλεται
στα
εργοστάσια για να μετατραπεί σε UF6.
Στα ορυχεία ουρανίου το μετάλλευμα του ουρανίου (με περιεκτικότητες
που μπορεί να καλύπτουν την περιοχή από 0,1 έως και 20% σε
U3O8) επεξεργάζεται συνήθως επιτόπου
με σκοπό την παρασκευή μιας εμπορικής μορφής ουρανιούχου συμπυκνώματος (concentrate), το
οποίο λόγω χρώματος και υφής είναι γνωστό ως κίτρινο κέικ (yellow cake).
Το κίτρινο κέικ τυπικά μπορεί να περιέχει 65% έως 85%
U3O8.
To U3O8
είναι μικτό οξείδιο (U3O8
= UO2·2UO3)
και αποτελεί τον συνήθη "τρόπο έκφρασης" της περιεκτικότητας σε ουράνιο
οποιουδήποτε μεταλλεύματός του (% U3O8).
Το κίτρινο κέικ αποτελεί τη μορφή με την οποία το ουράνιο αποστέλλεται
στα
εργοστάσια για να μετατραπεί σε UF6.
Η διαδικασία παραγωγής του κίτρινου κέικ εξαρτάται από το είδος του
μεταλλεύματος και
την περιεκτικότητά του σε ουράνιο. Το ουρανιούχο μετάλλευμα υφίσταται οξειδωτική
επεξεργασία σε όξινο (οξειδωτικό: Fe(III) ή MnO2) ή αλκαλικό
διάλυμα (οξειδωτικό: O2). Ακολουθούν
διαδικασίες διαχωρισμού με ιονανταλλακτικές
ρητίνες ή εκχυλίσεις.
Ο πιο απλός τρόπος εμπλουτισμού
και απαλλαγής από άλλα μέταλλα που συνήθως συνοδεύουν το ουράνιο (όπως θόριο, μολυβδαίνιο, βολφράμιο κ.α.) βασίζεται
στην εκχύλιση ισχυρά όξινου υδατικού διαλύματος νιτρικού ουρανυλίου, UO2(NO3)2,
με διάλυμα φωσφορικού τριβουτυλεστέρα [ (C4H9)3PO4,
TBT ] σε κηροζίνη. Σε ισχυρά όξινο (με ΗΝΟ3) υδατικό
διάλυμα το UO2(NO3)2
εκχυλίζεται από την ειδικώς ελαφρότερη οργανική φάση του ΤΒΤ, από την οποία
μπορεί να παραληφθεί (απαλλαγμένο από ακαθαρσίες άλλων μετάλλων) με επανεκχύλιση με καθαρό νερό.
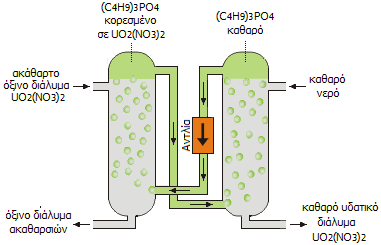
Η διαδικασία της εκχύλισης είναι
συνεχής και σχηματικά δείχνεται στο παραπλεύρως σχήμα.
Περισσότερες λεπτομέρειες πάνω στη χημεία της παραγωγής του
"κίτρινου κέικ" και σχετικό φωτογραφικό υλικό μπορούν να αναζητηθούν στην
εξαιρετική παρουσίαση του Καθηγητού Monhemius του
Royal School of Mines στο
Imperial College [Αναφ.
8].
Η μετατροπή
του κίτρινου κέικ
σε εξαφθοριούχο ουράνιο βασίζεται στην ακόλουθη αλληλουχία αντιδράσεων:
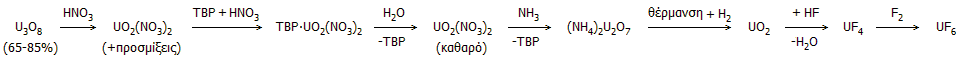
Το κίτρινο κέικ διαλύεται σε νιτρικό οξύ, οπότε όλο
το U3O8
μετατρέπεται σε
UO2(NO3)2
το οποίο στη
συνέχεια υφίσταται ένα επιπλέον καθαρισμό με εκχύλιση με φωσφορικό τριβουτύλιο,
όπως περιγράφηκε προηγουμένως. Στο καθαρό διάλυμα
UO2(NO3)2
προστίθεται αμμωνία και περίσσεια αμμωνιακών αλάτων, οπότε καθιζάνει κρυσταλλικό
ίζημα διουρανικού αμμωνίου, (ΝΗ4)2U2O7.
Το άλας αυτό θερμαίνεται σε ρεύμα υδρογόνου οπότε
διασπάται και μετατρέπεται στο οξείδιο
UO2.
Το UO2
με HF μετατρέπεται σε UF4, το οποίο τελικά οξειδώνεται με
ηλεκτρολυτικά παραγόμενο στοιχειακό φθόριο
προς
UF6.
Το UF6
αποστέλλεται στα εργοστάσια εμπλουτισμού σε κυλίνδρους
περιεκτικότητας περίπου 12 τόννων. Εκεί, οι κύλινδροι τοποθετούνται σε αυτόκλειστο
όπου θερμαίνονται και το περιεχόμενο UF6
αεριοποιείται και διοχετεύεται στο σύστημα ισοτοπικού διαχωρισμού. Μια πληρέστερη περιγραφή της παρασκευής, των ιδιοτήτων
και των τρόπων χειρισμού και φύλαξης του UF6
με πολύ καλό φωτογραφικό υλικό μπορεί να αναζητηθεί στις ιστοσελίδες του
Argonne National Laboratory (Illinois, ΗΠΑ)
[Αναφ. 9].
|

Κίτρινο κέικ (65-85%
U3O8) |
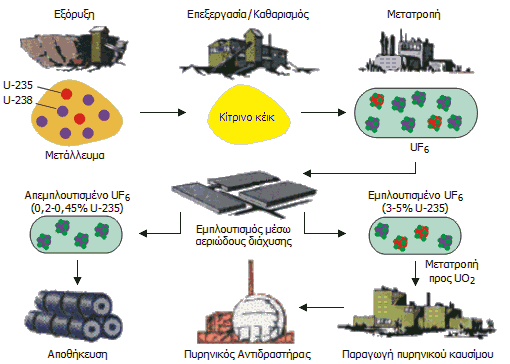
Σχηματική απεικόνιση παραγωγής
UF6
και πυρηνικών καυσίμων |
|

Κρύσταλλοι εξαφθοριούχου ουρανίου σε
υάλινη αμπούλα |
Πυρηνικά καύσιμα
|

Τυπική μορφή ράβδων
πυρηνικών καυσίμων. |
Το εμπλουτισμένο UF6
είναι πτητική ουσία και επομένως δεν μπορεί να χρησιμοποιηθεί ως πυρηνικό
καύσιμο. Για τον λόγο αυτό μετατρέπεται σε
UO2.
Αυτό το καστανόχρωμο οξείδιο είναι ένα εξαιρετικά σταθερό και δύστηκτο (σ.τ. ~2800ºC) κεραμικό υλικό και
επομένως είναι κατάλληλο για να καταστεί η "πηγή θερμότητας" κατά την πυρηνική
αντίδραση, χωρίς να υποστεί αλλοιώσεις.
Η μετατροπή του
εμπλουτισμένου UF6 σε εμπλουτισμένο
UO2 βασίζεται στην αντίδρασή του
σε υψηλή θερμοκρασία με υδρατμούς παρουσία υδρογόνου, σύμφωνα με την αλληλουχία
των αντιδράσεων:
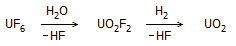
Το UO2
πιέζεται σε κυλινδρίσκους (pellets)
οι οποίοι επιστοιβάζονται σε σωλήνες από δύστηκτο κράμα ζιρκονίου (Zircaloy,
~98%
Zr) σχηματίζοντας τις "ράβδους καυσίμων" (fuel rods).
Το ζιρκόνιο είναι ένα δύστηκτο μέταλλο (σ.τ.
1852ºC), εξαιρετικά ανθεκτικό στη διάβρωση και
επιπλέον "διαφανές" στα νετρόνια, όλα απαραίτητες προϋπόθεσεις για τη δεδομένη
εφαρμογή του.
Δέσμες (bundles)
αυτών των ράβδων είναι οι τελικές "εμπορικές" μορφές των πυρηνικών καυσίμων ουρανίου. Οι
δέσμες αυτές εισάγονται στους πυρηνικούς αντιδραστήρες, προκειμένου
να δεχθούν τη ροή των νετρονίων και να ακολουθήσει η αυτοσυντηρούμενη πυρηνική
αντίδραση που τις μετατρέπει σε πηγές θερμότητας.
 Φυσικές
και χημικές ιδιότητες του
εξαφθοριούχου ουρανίου
Φυσικές
και χημικές ιδιότητες του
εξαφθοριούχου ουρανίου
Για τους λόγους που αναφέρθηκαν
παραπάνω το
UF6
είναι η μορφή που πρέπει να αποκτήσει το φυσικό ουράνιο για να μπορέσει να
ακολουθήσει η διαδικασία εμπλουτισμού του σε ισότοπο U-235.
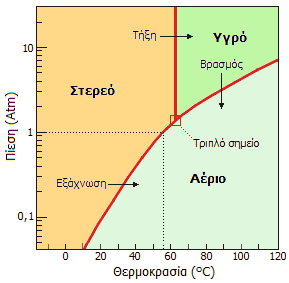
Από το διάγραμμα φάσεων του UF6
(αριστερά) φαίνεται ότι
σε ατμοσφαιρική πίεση, κάτω από τους 57ºC
το UF6 είναι στερεό, ενώ σε μεγαλύτερες θερμοκρασίες υφίσταται εξάχνωση, δηλαδή
μετατρέπεται σε αέριο χωρίς να μεσολαβήσει η υγρή φάση
[Αναφ. 10].
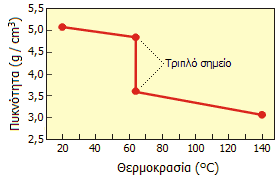 Μια
χαρακτηριστική φυσική ιδιότητα του UF6 είναι μεγάλη μείωση της
πυκνότητάς του όταν από στερεό (d = 5,09 g/cm3 στους 27ºC)
μετατρέπεται σε υγρό (d = 3,26 g/cm3 στους 120ºC).
Αυτό συνεπάγεται μεγάλη αύξηση (>50%) του όγκου του UF6
κατά την τήξη του, που πρέπει να λαμβάνεται υπόψη για να αποφευχθεί ρήξη των κυλίνδρων στους οποίους
φυλάσσεται κατά την αύξηση της θερμοκρασίας του περιεχομένου τους [Αναφ. 11].
Μια
χαρακτηριστική φυσική ιδιότητα του UF6 είναι μεγάλη μείωση της
πυκνότητάς του όταν από στερεό (d = 5,09 g/cm3 στους 27ºC)
μετατρέπεται σε υγρό (d = 3,26 g/cm3 στους 120ºC).
Αυτό συνεπάγεται μεγάλη αύξηση (>50%) του όγκου του UF6
κατά την τήξη του, που πρέπει να λαμβάνεται υπόψη για να αποφευχθεί ρήξη των κυλίνδρων στους οποίους
φυλάσσεται κατά την αύξηση της θερμοκρασίας του περιεχομένου τους [Αναφ. 11].
Το UF6
δρα
οξειδωτικά και είναι ισχυρό οξύ
κατά Lewis.
Απαιτεί ιδιαίτερες προφυλάξεις κατά τη χρήση του και πρέπει να αποφεύγεται κάθε
επαφή του με το δέρμα, όπως και η εισπνοή ατμών του. Κυριότερος λόγος της
χημικής επικινδυνότητάς του είναι η τοξικότητα του ουρανίου, αλλά και το ότι
αντιδρά με το νερό σχηματίζοντας το διαβρωτικό και τοξικό υδροφθόριο σύμφωνα με την αντίδραση:
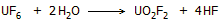
To
UF6
διαλύεται σε οργανικούς διαλύτες, αλλά φαίνεται ότι μόνο τα
διαλύματά του σε υπερφθοριωμένους υδρογονάνθρακες είναι σταθερά.
Δεν αντιδρά με τα μέταλλα Ni και Al
λόγω σχηματισμού προστατευτικού στρώματος αδιάλυτων φθοριούχων αλάτων των
μετάλλων και μπορεί να φυλαχθεί για μεγάλα χρονικά διαστήματα σε καλά σφραγισμένους
κυλίνδρους από ανοξείδωτο χάλυβα.
Επικινδυνότητα του
εξαφθοριούχου ουρανίου
Το απεμπλουτισμένο
εξαφθοριούχο ουράνιο (depleted UF6,
DUF6) είναι
το κύριο παραπροϊόν της διαδικασίας παραγωγής εμπλουτισμένου ουρανίου.
Για την παραγωγή 1 kg
εμπλουτισμένου ουρανίου κατάλληλου ως πυρηνικό καύσιμο (5% σε U-235)
απαιτούνται 11,8 kg φυσικού ουρανίου και απομένουν 10,8 kg
απεμπλουτισμένου ουρανίου, δηλαδή περίπου το 92% του "φυσικού" UF6,
που εισέρχεται σε ένα εργοστάσιο παραγωγής εμπλουτισμένου ουρανίου, εξέρχεται ως παραπροϊόν.
Το
DUF6
φυλάσσεται σε
ειδικά κατασκευασμένους σφραγισμένους κυλίνδρους χωρητικότητας 12 τόννων,
οι οποίοι πρέπει να κατασκευάζονται
και να συντηρούνται με βάση αυστηρότατες προδιαγραφές (ANSI
N14.1-2001). Για παράδειγμα, μια από τις
κατασκευαστικές απαιτήσεις
είναι ότι πρέπει να παραμένουν
άθικτοι όταν θερμανθούν με το περιεχόμενό τους στους 800ºC
για 30 s [Αναφ. 12].
Η σώρευση χιλιάδων κυλίνδρων (από τη δεκαετία του 1940 μέχρι σήμερα) με
DUF6 αποτελεί οικονομικό και περιβαλλοντικό πρόβλημα.
Το κόστος φύλαξης και συντήρησης των κυλίνδρων είναι μεγάλο. Σε μια έκθεση
της Υπηρεσία Περιβάλλοντος των ΗΠΑ του 2001 αναφέρεται ότι στα εργοστάσια
παραγωγής εμπλουτισμένου ουρανίου των ΗΠΑ (στις πόλεις Portsmouth, Paducah
και Oak Ridge), υπήρχαν αποθηκευμένοι 700.000 τόννοι
DUF6
σε 57.700 κυλίνδρους
[Αναφ. 13].
|

(α) |

(β) |

(γ) |
|
Το απεμπλουτισμένο
εξαφθοριούχο ουράνιο (DUF6) αποθηκεύεται
σε χαλύβδινους κυλίνδρους διαμέτρου 1,2 m
και χωρητικότητας περίπου 12 τόννων:
(α) Ειδικό όχημα μεταφοράς των κυλίνδρων.
(β) Υπαίθριος χώρος με επιφάνεια επιστρωμένη με τσιμέντο, όπου
αποθηκεύονται χιλιάδες κυλίνδρων με DUF6.
(γ) Οξειδωμένος κύλινδρος στον οποίο έχει διαπιστωθεί διαρροή
DUF6. |
Η αντίδραση του
UF6
με το νερό το καθιστά εξαιρετικά επικίνδυνη ένωση λόγω της τοξικότητας του
παραγόμενων προϊόντων (HF, UO2F2)
και της σύγχρονης έκλυσης μεγάλων ποσών θερμότητας. Το υδροφθόριο ερεθίζει
τους πνεύμονες και μπορεί να προκαλέσει πνευμονικό οίδημα, ενώ οι ενώσεις του
ουρανίου είναι νεφροτοξικές.
'Εχουν αναφερθεί αρκετά
ατυχήματα στα εργοστάσια παραγωγής UF6
ή εμπλουτισμού ουρανίου. Το 1944, κατά τη θέρμανση ενός κυλίνδρου
UF6
με ατμό, έσπασε μια συγκόλληση του κυλίνδρου με αποτέλεσμα
την έκλυση 200 kg
UF6,
τα οποία αντέδρασαν με τους ατμούς ύδατος με αποτέλεσμα την παραγωγή μεγάλης
ποσότητας HF που προκάλεσε τον θάνατο δύο ατόμων.
Το 1978, ένας κύλινδρος UF6
έσπασε σε μια αποθήκη πυρηνικών καυσίμων χωρίς θύματα. Σε ένα άλλο ατύχημα, το 1986,
ένα άτομο πέθανε από εισπνοή αερίου HF από ρήξη ενός κυλίνδρου, άλλα 31 άτομα
που εκτέθηκαν στους ατμούς δεν παρουσίασαν βλάβες σε βάθος χρόνου
[Αναφ. 14].
 Διαρροή UF6
από τους κυλίνδρους θα έχει ως συνέπεια τη ρύπανση του υδροφόρου ορίζοντα με
φθοριούχα και με ενώσεις του τοξικού ουρανίου. Το γεγονός αυτό επιβάλλει
συνεχείς ελέγχους της κατάστασης των κυλίνδρων αποθήκευσης του UF6,
κάτι που αποτελεί μια επικίνδυνη και ιδιαίτερα δαπανηρή διαδικασία [Αναφ. 15].
'Eχουν προταθεί διάφορα σχήματα χημικής αντιμετώπισης, όπως π.χ. δέσμευση των
φθοριούχων ως HF και CaF2
και του (απεμπλουτισμένου) ουρανίου στη μορφή του οξειδίου UO2.
Διαρροή UF6
από τους κυλίνδρους θα έχει ως συνέπεια τη ρύπανση του υδροφόρου ορίζοντα με
φθοριούχα και με ενώσεις του τοξικού ουρανίου. Το γεγονός αυτό επιβάλλει
συνεχείς ελέγχους της κατάστασης των κυλίνδρων αποθήκευσης του UF6,
κάτι που αποτελεί μια επικίνδυνη και ιδιαίτερα δαπανηρή διαδικασία [Αναφ. 15].
'Eχουν προταθεί διάφορα σχήματα χημικής αντιμετώπισης, όπως π.χ. δέσμευση των
φθοριούχων ως HF και CaF2
και του (απεμπλουτισμένου) ουρανίου στη μορφή του οξειδίου UO2.
Θα
πρέπει να σημειωθεί ότι πέραν των χημικών κινδύνων από την αποθήκευση των
κυλίνδρων
DUF6
και μάλιστα σε υπαίθριους χώρους, οι κύλινδροι αυτοί αποτελούν και ραδιολογικό
κίνδυνο, αφού αποτελούν πηγές εκπομπής νετρονίων και ακτινοβολίας γ χαμηλής στάθμης.
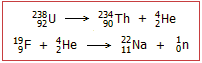
Η εκπομπή νετρονίων εμφανίζεται ειδικά στις φθοριούχες ενώσεις του ουρανίου και
οφείλεται στην παραπλεύρως αλληλουχία πυρηνικών αντιδράσεων, όπου συμμετέχουν οι
πυρήνες του φθορίου.
|

Ρύγχος βλήματος 30 mm από απεμπλουτισμένο
ουράνιο . |
Χρήσεις του απεμπλουτισμένου εξαφθοριούχου ουρανίου
|

Βλήματα με διατρητική
κεφαλή απεμπλουτισμένου ουρανίου. |
Το
DUF6
ως ένωση δεν έχει καμία χρησιμότητα, αλλά αποτελεί την πρώτη ύλη παραγωγής μεταλλικού
απεμπλουτισμένου
ουρανίου (depleted uranium, DU) και ενώσεών του. Δεδομένης της ευρύτατης παραγωγής
εμπλουτισμένου ουρανίου για πυρηνικά καύσιμα και πυρηνικά όπλα, εκτιμάται
ότι τα υπάρχοντα παγκόσμια αποθέματα DU ξεπερνούν το 1,2
εκατομμύρια τόννους.
Οι
"πολιτικές" χρήσεις του DU είναι περιορισμένες, έτσι π.χ.
λόγω του μεγάλου ειδικού βάρους, ως μέταλλο χρησιμοποιείται ως "έρμα"
σταθεροποίησης σε αεροσκάφη και
γενικά σε περιπτώσεις που τα αντίβαρα πρέπει να καταλαμβάνουν μικρό όγκο. 'Ενα
Boeing 747 χρειάζεται έρμα 1500 kg
DU. Οι
χημικές ενώσεις του ουρανίου που διατίθενται στο εμπόριο, στο σύνολό τους
προέρχονται από DU. Οξείδια του ουρανίου χρησιμοποιούνται ως εξαιρετικά δύστηκτα κεραμικά υλικά και για τον
χρωματισμό υάλων και πορσελάνης. Το νιτρικό ουρανύλιο UO2(NO3)2 χρησιμοποιήθηκε
παλαιότερα στη φωτογραφική τεχνική και το οξικό ουρανύλιο UO2(CH3COO)2
αποτελεί κλασικό αντιδραστήριο για την ανίχνευση
του νατρίου, επειδή σχηματίζει το δυσδιάλυτο μικτό άλας NaZn(UO2)3(CH3COO)9·xH2O
(x = 6-9).
Αντίθετα, οι στρατιωτικές εφαρμογές του
μεταλλικού DU αφθονούν. Χρησιμοποιείται για κατασκευή ανθεκτικότατων θωρακίσεων στρατιωτικών οχημάτων,
όπως επίσης βομβών και βλημάτων εξαιρετικά μεγάλης διατρητικής ικανότητας,
αντικαθιστώντας άλλα δαπανηρότερα μέταλλα με παρόμοιες ιδιότητες όπως είναι το βολφράμιο
[Αναφ. 16]. Το
DU συνδυάζει πλεονεκτήματα
όπως:
(α)
'Εχει μεγάλη πυκνότητα (2,5 φορές πιο πυκνό από τον σίδηρο)
και σκληρότητα. 'Οταν χρησιμοποιηθεί ως ρύγχος (μύτη) στα βλήματα και στις βόμβες
αυξάνει κατά πολύ τη διατρητική ικανότητά τους, αφού μπορούν πλέον να διαπεράσουν παχιές
πλάκες από σίδηρο και τσιμέντο.
(β)
"Αυτοεκρήγνυται". Ακόμη και χωρίς εκρηκτική γόμωση, τα βλήματα από ουράνιο κατά την
πρόσκρουση εκρήγνυνται και αναπτύσσουν υψηλές θερμοκρασίες λόγω κονιοποίησης του
ουρανίου και ακαριαίας ανάφλεξης της σκόνης του (οξείδωση από το ατμοσφαιρικό οξυγόνο), κάτι που αυξάνει την καταστροφική τους
δράση.
(γ)
Μικρό κόστος, αφού αποτελεί ένα άφθονο σε ποσότητα και ουσιαστικά άχρηστο παραπροϊόν της
παραγωγής πυρηνικών καυσίμων.
Φαίνεται ότι η
αξιοποίηση του DU στην κατασκευή συμβατικών οπλικών
συστημάτων με επακόλουθο τη διασπορά του στα πεδία μαχών, μπορεί να θεωρηθεί
ως "επικερδής" και "αποτελεσματικός"
τρόπος απαλλαγής τουλάχιστον από ένα μέρος από τα τεράστια και "ανεπιθύμητα" αποθέματα
DUF6 [Αναφ.
17, 18].
|
Σχετικά με τη χρήση του όρου "απεμπλουτισμένο ουράνιο"
|
Μορφή
ουρανίου |
Ιδιότητα |
U-234 |
U-235 |
U-238 |
Σύνολο |
|
Φυσικό
ουράνιο |
%
περιεκτικότητα |
0,0053 |
0,711 |
99,275 |
100 |
|
Ραδιενέργεια,
Bq/g* |
12356 |
568 |
12356 |
25280 |
|
Εμπλουτισμένο ουράνιο
(3,5% σε
U-235) |
%
περιεκτικότητα |
0,02884 |
3,5 |
99,275 |
100 |
|
Ραδιενέργεια,
Bq/g |
66703 |
2800 |
12005 |
81508 |
|
Απεμπλουτισμένο ουράνιο (παραπροϊόν παραγωγής του
προηγούμενου) |
%
περιεκτικότητα |
0,0008976 |
0,2 |
99,799 |
100 |
|
Ραδιενέργεια,
Bq/g |
2076 |
160 |
12420 |
14656 |
|
*
Becquerel
(Bq):
Μονάδα ραδιενέργειας που αντιστοιχεί στον αριθμό διασπώμενων
πυρήνων ραδιενεργού υλικού σε ένα δευτερόλεπτο |
Συχνά, σε αναφορές
στο απεμπλουτισμένο ουράνιο που γίνονται από τα μέσα μαζικής
ενημέρωσης, αφήνεται να εννοηθεί ότι τούτο αποτελεί μια
ιδιαίτερα επικίνδυνη και τοξική μορφή του ουρανίου. Κάτι τέτοιο βέβαια δεν ισχύει. Το
DU δεν διαφέρει
ουσιαστικά σε καμία φυσική, χημική ή τοξικολογική ιδιότητα από το φυσικό
ουράνιο. Το DU απλώς περιέχει το ισότοπο
U-235
(και μαζί με αυτό και το
U-234)
σε μικρότερη αναλογία απ' ό,τι το φυσικό ουράνιο και για τον λόγο αυτό
είναι και λιγότερο ραδιενεργό, χωρίς αυτό να σημαίνει ότι είναι λιγότερο επικίνδυνο
για την υγεία όσων έρχονται σε επαφή με αυτό
και ιδιαίτερα όσων εισπνεύσουν μικροσωματίδια που περιέχουν οξείδια ή
άλλες ενώσεις του.
Στον
πίνακα δείχνονται συγκριτικά οι τυπικές ισοτοπικές συστάσεις και η
ραδιενέργεια των διαφόρων μορφών ουρανίου [Αναφ.
19]. |
Πηγές από το Διαδίκτυο - Βιβλιογραφία
1. Merck Index 12th edition
(1996): "Uranium Hexafluoride".
2. (α) Wikipedia: "Martin
Heinrich Klaproth".
(β) Wikipedia: "Eugène-Melchior Péligot".
3. (α) Wikipedia: "Uranium".
(β) Federation of American Scientists, Special Weapon Primer: "Uranium
production". (γ) World Nuclear Association: "Uranium
Enrichment". (δ) The Encyclopedia of Earth: "Uranium
enrichment".
4. Nininger RD: "Minerals
for Atomic Energy: The Uranium ore minerals" (D. Van Nostrand Company, Inc.
New York, 1954).
5. Institute for Energy and
Environmental Research (IEER): "Uranium:
Its Uses and Hazards".
6. (α) World
Nuclear Association: "Some
Physics on Uranium". (β) Hyperphysics Web Page
(Georgia State University): "Uranium-235
Fission".
7. (α) Institute for
Science and International Security: "What
is a Gas Centrifuge?".
(β) Wikipedia: "Enriched
Uranium".
8.
Monhemius J (Royal Shcool of Mines, Imperial College, London): "Processing
Uranium Ores to produce Yellowcake" (αρχείο
PDF, 2,18 MB).
9.
Argonne National Laboratory (ANL): "Depleted
UF6: The
Uranium Fuel Cycle".
10.
Argonne National Laboratory (ANL): "Properties
of Uranium Hexafluoride (UF6)".
11.
Argonne National Laboratory (ANL): "UF6
cylinders:
Full limit criteria".
12. Werkoff F, Bontemps
A, Maréchal A: "On controversy of behaviour of UF6
cylinders exposed to fire: deeper examination of experimental results",
Packaging, Transport, Storage and Security of Radioactive Material, 17:165-171
(2006) (Abstract).
13. U.S. Environmental Protection Agency: "Notice
of Intent To Prepare an Environmental Impact Statement for Depleted Uranium
Hexafluoride Conversion Facilities"
(September, 2001).
14.
Subcommittee on Acute Exposure Guideline Levels, Committee on Toxicology,
National Research Council:
"Appendix
5:
Uranium Hexafluoride Acute Exposure Guideline Levels",
Acute Exposure Guideline
Levels for Selected Airborne Chemicals: Volume 4,
The National Academic
Press (2004)
15. Argonne National Laboratory (ANL):
"Final programming environmental impact for alternative
strategies for the long-term management and use of
depleted uranium hexafluoride (Summary)", April, 1999 (αρχείο
PDF, 473 KB).
16. Wikipedia: "Depleted
uranium".
17. Maeda A, Saruta S, Inamori K, ICTI: "The
Excessive Use of Weapons and Banned Weapons - The Use of Depleted Uranium (DU)
Weapons".
18.
Pesic I : "Depleted
Uranium: Ethics of the Silver Bullet",
School of Engineering, Santa Clara University.
19. World
Informations Service on Energy (WISE): "Uranium
Radiation Properties".
'Αλλες
ενδιαφέρουσες ιστοσελίδες για το εξαφθοριούχου ουράνιο και το απεμπλουτισμένο
ουράνιο
|
Αποποίηση
ευθυνών:
Έχει καταβληθεί κάθε προσπάθεια για να εξασφαλισθεί η ορθότητα των
πληροφοριών που περιλαμβάνονται σε αυτή τη σελίδα, ωστόσο ο έχων την
επιμέλεια της σελίδας αυτής και το Τμήμα Χημείας δεν αναλαμβάνουν τη
νομική ευθύνη για τυχόν σφάλματα, παραλείψεις ή ανακριβείς πληροφορίες.
Επιπλέον, το Τμήμα Χημείας δεν εγγυάται την ορθότητα των αναφερόμενων σε
εξωτερικές ιστοσελίδες, ούτε η αναφορά μέσω συνδέσμων (links) στις ιστοσελίδες αυτές, υποδηλώνει ότι το Τμήμα
Χημείας επικυρώνει ή καθ' οιονδήποτε τρόπο αποδέχεται το περιεχόμενό
τους. |



 Ορισμένες
από τις φυσικές ιδιότητες του ουρανίου δίνονται στον παραπλεύρως πίνακα. Από
χημική άποψη το ουράνιο είναι χημικώς δραστικό στοιχείο με πιο σταθερές οξειδωτικές
καταστάσεις τις +4 και +6. Σε λεπτό διαμερισμό (π.χ. ως σκόνη) αντιδρά αργά με το νερό με έκλυση
υδρογόνου και είναι πυροφόρο, δηλ. μπορεί να αναφλεγεί αυτόματα οξειδούμενο από
το οξυγόνο του αέρα (π.χ. κατά τη μηχανουργική επεξεργασία). Σε συμπαγή μορφή το ουράνιο οξειδώνεται αργά στον αέρα και καλύπτεται από ένα μαύρο στρώμα
οξειδίων.
Ορισμένες
από τις φυσικές ιδιότητες του ουρανίου δίνονται στον παραπλεύρως πίνακα. Από
χημική άποψη το ουράνιο είναι χημικώς δραστικό στοιχείο με πιο σταθερές οξειδωτικές
καταστάσεις τις +4 και +6. Σε λεπτό διαμερισμό (π.χ. ως σκόνη) αντιδρά αργά με το νερό με έκλυση
υδρογόνου και είναι πυροφόρο, δηλ. μπορεί να αναφλεγεί αυτόματα οξειδούμενο από
το οξυγόνο του αέρα (π.χ. κατά τη μηχανουργική επεξεργασία). Σε συμπαγή μορφή το ουράνιο οξειδώνεται αργά στον αέρα και καλύπτεται από ένα μαύρο στρώμα
οξειδίων.



 Ισοτοπική σύνθεση και ραδιενέργεια φυσικού
ουρανίου
Ισοτοπική σύνθεση και ραδιενέργεια φυσικού
ουρανίου Το χρήσιμο (ως πυρηνικό καύσιμο) ισότοπο του
ουρανίου είναι το U-235. 'Οταν οι πυρήνες του U-235 βομβαρδιστούν με τα ονομαζόμενα "αργά" ή "θερμικά"
νετρόνια, υφίστανται σχάση (fission) με έκλυση μεγάλων ποσών ενέργειας κυρίως υπό τη
μορφή θερμότητας. Η γενική αντίδραση έχει τη μορφή:
Το χρήσιμο (ως πυρηνικό καύσιμο) ισότοπο του
ουρανίου είναι το U-235. 'Οταν οι πυρήνες του U-235 βομβαρδιστούν με τα ονομαζόμενα "αργά" ή "θερμικά"
νετρόνια, υφίστανται σχάση (fission) με έκλυση μεγάλων ποσών ενέργειας κυρίως υπό τη
μορφή θερμότητας. Η γενική αντίδραση έχει τη μορφή:



 Στα ορυχεία ουρανίου το μετάλλευμα του ουρανίου (με περιεκτικότητες
που μπορεί να καλύπτουν την περιοχή από 0,1 έως και 20% σε
Στα ορυχεία ουρανίου το μετάλλευμα του ουρανίου (με περιεκτικότητες
που μπορεί να καλύπτουν την περιοχή από 0,1 έως και 20% σε
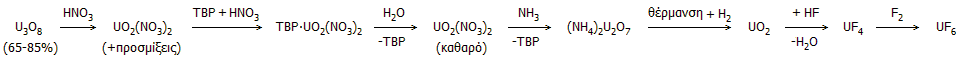




 Φυσικές
και χημικές ιδιότητες του
εξαφθοριούχου ουρανίου
Φυσικές
και χημικές ιδιότητες του
εξαφθοριούχου ουρανίου Μια
χαρακτηριστική φυσική ιδιότητα του UF6 είναι μεγάλη μείωση της
πυκνότητάς του όταν από στερεό (d = 5,09 g/cm3 στους 27
Μια
χαρακτηριστική φυσική ιδιότητα του UF6 είναι μεγάλη μείωση της
πυκνότητάς του όταν από στερεό (d = 5,09 g/cm3 στους 27


 Διαρροή UF6
από τους κυλίνδρους θα έχει ως συνέπεια τη ρύπανση του υδροφόρου ορίζοντα με
φθοριούχα και με ενώσεις του τοξικού ουρανίου. Το γεγονός αυτό επιβάλλει
συνεχείς ελέγχους της κατάστασης των κυλίνδρων αποθήκευσης του UF6,
κάτι που αποτελεί μια επικίνδυνη και ιδιαίτερα δαπανηρή διαδικασία [
Διαρροή UF6
από τους κυλίνδρους θα έχει ως συνέπεια τη ρύπανση του υδροφόρου ορίζοντα με
φθοριούχα και με ενώσεις του τοξικού ουρανίου. Το γεγονός αυτό επιβάλλει
συνεχείς ελέγχους της κατάστασης των κυλίνδρων αποθήκευσης του UF6,
κάτι που αποτελεί μια επικίνδυνη και ιδιαίτερα δαπανηρή διαδικασία [
