|
 |
|
Δύο
Βυζαντινοί αυτοκράτορες, ο
Ιουλιανός ο "Παραβάτης"
(332-363) (αριστερά) και στη συνέχεια ο διάδοχός του ο
Ιωβιανός
(331-364) (δεξιά), πιθανώς υπήρξαν θύματα δηλητηρίασης από
CO
από μαγκάλι
[Αναφ. 1δ].
Στον δεύτερο η δηλητηρίαση αυτή στοίχισε τη ζωή του. |
Ιστορία
και ανακάλυψη του μονοξειδίου του άνθρακα [Αναφ. 1]
Οι τοξικές και θανατηφόρες ιδιότητες του μονοξειδίου του άνθρακα (CO)
είναι γνωστές από την αρχαιότητα, καθώς η χρήση κάρβουνου και ξύλων για
θέρμανση σε μη καλά αεριζόμενα δωμάτια προκαλούσε αρχικά πονοκέφαλο, ζάλη,
δύσπνοια, λιποθυμία και τελικά τον θάνατο. Ο
Γαληνός είχε σωστά υποθέσει ότι οι δηλητηριώδεις ατμοί από μισοαναμμένες φωτιές
προκαλούσαν αλλαγές στη σύσταση του αέρα.
Στην αρχαιότητα χρησιμοποιούσαν τον εγκλεισμό σε μικρά κλειστά λουτρά με μισοαναμμένα
κάρβουνα για την εκτέλεση ληστών. Ακόμη, πιθανολογείται ότι δύο Βυζαντινοί
αυτοκράτορες, ο
Ιουλιανός ο "Παραβάτης"
(332-363) και στη συνέχεια ο διάδοχός του ο
Ιωβιανός
(331-364), υπήρξαν θύματα δηλητηρίασης από μονοξείδιο του άνθρακα (από
μαγκάλια), από την οποία ο πρώτος συνήλθε, ενώ ο δεύτερος έχασε τη ζωή του
[Αναφ. 1δ].
 Σε πιο
πρόσφατη εποχή, το
1940,
το μονοξείδιο του άνθρακα των καυσαερίων ειδικά
διασκευασμένων αυτοκινήτων (των περίφημων "Gaswagen")
χρησιμοποιήθηκε από το ναζιστικό
καθεστώς της Γερμανίας στα πλαίσια της ευγονικής εκστρατείας για την ομαδική
"ευθανασία" χιλιάδων
εκ γενετής ανάπηρων, πνευματικά καθυστερημένων και ψυχασθενών ατόμων.
Σε πιο
πρόσφατη εποχή, το
1940,
το μονοξείδιο του άνθρακα των καυσαερίων ειδικά
διασκευασμένων αυτοκινήτων (των περίφημων "Gaswagen")
χρησιμοποιήθηκε από το ναζιστικό
καθεστώς της Γερμανίας στα πλαίσια της ευγονικής εκστρατείας για την ομαδική
"ευθανασία" χιλιάδων
εκ γενετής ανάπηρων, πνευματικά καθυστερημένων και ψυχασθενών ατόμων.
Κατά τον 13ο αιώνα, ο Ισπανός αλχημιστής
Arnaldus de Villa Nova
(1235-1311), έκανε μια αναφορά για κάποιο δηλητηριώδες αέριο που παραγόταν κατά την ατελή
καύση του ξύλου. Το 1664, ο διάσημος Φλαμανδός φυσιολόγος και
φυσικός
Johann Baptista van Helmont (1579-1644), ο οποίος μελέτησε πολλά
αέρια και καθιέρωσε τον όρο gas για τα αέρια από την ελληνική λέξη 'χάος', έγραψε
για κάποιο αέριο gas carbonum (προφανώς μίγμα CO + CO2),
το οποίο παρ' ολίγο να του κοστίσει τη ζωή.
Το 1776 ο Γάλλος χημικός
Joseph Marie François
de Lassone
(1717-1788)
παρασκεύασε μονοξείδιο του άνθρακα με θέρμανση οξειδίου του ψευδαργύρου με κωκ
(ZnO + C
 Zn +
CO), αλλά εσφαλμένα υπέθεσε ότι το αέριο ήταν υδρογόνο, επειδή
καιγόταν με φλόγα γαλάζιου χρώματος παρόμοιου με εκείνου της φλόγας υδρογόνου.
Zn +
CO), αλλά εσφαλμένα υπέθεσε ότι το αέριο ήταν υδρογόνο, επειδή
καιγόταν με φλόγα γαλάζιου χρώματος παρόμοιου με εκείνου της φλόγας υδρογόνου.
H ανακάλυψη του μονοξειδίου του άνθρακα και η διάκρισή του από το διοξείδιο
του άνθρακα αποδίδεται στον διάσημο 'Αγγλο χημικό και θεολόγο, όπως και
τελευταίο υπερασπιστή της "φλογιστικής" θεωρίας,
Joseph Pristley
(1733-1804). Το 1800, πρώτος ο Σκωτσέζος χημικός και ανατόμος
William Cumberland Cruikshank
(1745-1800),
προσδιόρισε ότι πρόκειται για αέριο που αποτελείται από άνθρακα και οξυγόνο.
To 1846, o Γάλλος φυσιολόγος
Claude
Bernard
(1813-1878) μελέτησε συστηματικά τις τοξικές
ιδιότητες
του
CO
χρησιμοποιώντας σκύλους ως
πειραματόζωα.
Το
μονοξείδιο του άνθρακα έχει χαρακτηρισθεί ως
σιωπηλός δολοφόνος
(silent killer), επειδή είναι ένα
τελείως άοσμο αέριο
και τα αρχικά συμπτώματα
της δηλητηρίασης που προκαλεί, συχνά συγχέονται με εκείνα ενός απλού κρυολογήματος. Είναι ένα
αέριο το οποίο μπορεί εύκολα να δημιουργηθεί στα σπίτια που θερμαίνονται με την
καύση οργανικών υλικών (ξύλων, κάρβουνο) σε περιπτώσεις κακής συντήρησης των
απαγωγών των αερίων καύσης ή κάποιων διαρροών. Πολλές περιπτώσεις
δηλητηριάσεων έχουν συμβεί σε κλειστά γκαράζ, όταν αφήνεται σε λειτουργία η
μηχανή των αυτοκινήτων. Στις ΗΠΑ εκτιμάται ότι κάθε
χρόνο κατά
μέσον όρο 500 άτομα χάνουν τη ζωή τους εξαιτίας του.
Στην Ελλάδα,
το θέμα της προστασίας έναντι του μονοξειδίου του άνθρακα ήλθε στην
επικαιρότητα λόγω
της στροφής μεγάλου μέρους του πληθυσμού στη θέρμανση με καύση ξύλου ή
διαφόρων προϊόντων του (pellets), εξαιτίας του δυσβάσταχτου πλέον κόστους του
πετρελαίου για τα συστήματα κεντρικής θέρμανσης.
 |
 |

Φλόγα υδρογόνου
(πηγή) |

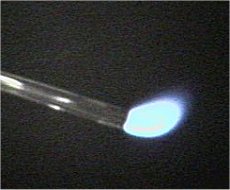
Φλόγα
μονοξειδίου του άνθρακα (πηγή) |
 |
|
Από αριστερά προς τα δεξιά: (α)
William Cumberland Cruikshank
(1745-1800): Σκωτσέζος χημικός και ανατόμος που πρώτος ανέφερε
ότι το CO είναι ένωση άνθρακα και οξυγόνου. (β)
Claude Bernard
(1813-1878): Ο Γάλλος φυσιολόγος που μελέτησε την τοξικότητα του
CO. (γ),(δ): Φλόγες καύσης Η2
και CO. Και τα δύο αέρια καιόμενα στον
αέρα παρέχουν φλόγες με σχεδόν ίδιο χρώμα. (ε)
Émile François Zola
(1840-1902), διάσημος
Γάλλος συγγραφέας, μάρτυρας υπεράσπισης στην περιβόητη υπόθεση
Dreyfus.
Θα πρέπει να είναι το διασημότερο θύμα του CO. |
|
 |
 |
|
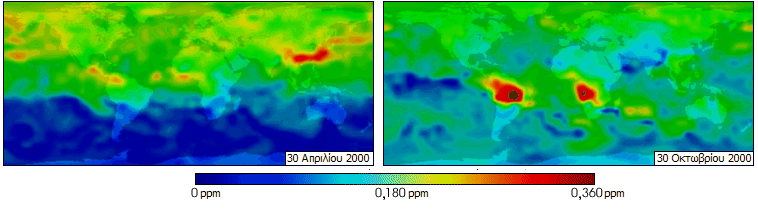
Συγκέντρωση CO στην ατμόσφαιρα, όπως
μετρήθηκε από τον Kαναδικό δορυφόρο MOPITT
(Meaurements
Of Pollution In The Troposphere)
στις αναγραφόμενες ημερομηνίες του 2000. Οι μεγάλες
συγκεντρώσεις κατά πάσα πιθανότητα οφείλονται σε τοπικές δασικές
πυρκαγιές [Αναφ. 2γ]. |
|
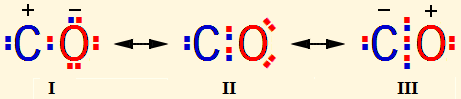
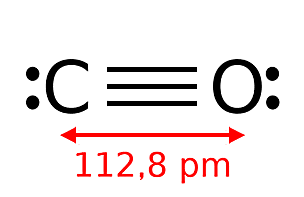
Δομές συντονισμού του
CO. Οι θέσεις που δείχνονται αποτελούν
"στιγμιότυπα", αφού τα ηλεκτρόνια αυτά είναι
διάχυτα (εναλλάσσουν θέσεις) στα
διάφορα δεσμικά μη δεσμικά τροχιακά (ασύζευκτα ζεύγη
ηλεκτρονίων). Η δομή ΙΙΙ
(τριπλού δεσμού) είναι η επικρατέστερη. |
|

Αυτοκίνητο
της εποχής του 2ου Παγκοσμίου Πολέμου με προσαρμοσμένη στο πίσω
μέρος τη συσκευή αεροποίησης (gazogen) στερεών καυσίμων. |
|
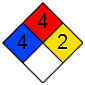
ΠΡΟΣΟΧΗ:
Οι αντιδράσεις παρασκευής μικροποσοτήτων CO
όπως
αυτές που παρουσιάζονται στις παραπάνω φωτογραφίες δεν παρουσιάζουν κάποια
επικινδυνότητα, αρκεί να μην επιχειρήσει κανείς να εισπνεύσει απ' ευθείας το
εκλυόμενο αέριο
-Μία εισπνοή
καθαρού CO (π.χ. για να διαπιστωθεί ότι είναι άοσμο) αρκεί για να επιφέρει
τον θάνατο-. Ωστόσο, τα χημικά εργαστήρια στα οποία γίνεται συχνή
χρήση CO (κυρίως από φιάλες του αερίου) θα πρέπει να είναι
εξοπλισμένα με ηλεκτρονικούς ανιχνευτές του αερίου που με ηχητικό σήμα
προειδοποιούν για την παρουσία επικίνδυνων επιπέδων CO στην ατμόσφαιρα.
Πρέπει να τονιστεί ότι διαρροές του μονοξειδίου του άνθρακα δεν γίνoνται αντιληπτές
και τα πρώτα συμπτώματα δηλητηρίασης (πονοκέφαλος, ζάλη, εξάντληση, καταρροή) μπορούν εύκολα
να παρερμηνευθούν και να θεωρηθούν ως φυσιολογικό αποτέλεσμα μιας
ημέρας κουραστικής εργασίας ή σαν ένα κοινό κρυολόγημα.
Τα μέτρα ασφάλειας για τον
χειρισμό του μονοξειδίου του άνθρακα που ισχύουν σε ένα πανεπιστημιακό
εργαστήριο (University of Pensylvania) είναι εντυπωσιακά για την αυστηρότητά
τους και μπορούν να
αναζητηθούν εδω: "GUIDELINES FOR CARBON MONOXIDE GAS USAGE IN LABORATORIES.
|
|
|
Αριστερά: Διαβίβαση αέρα
μέσω σωλήνα με θερμαινόμενα ρηνίσματα χαλκού προκαλεί αμαύρωσή
τους λόγω σχηματισμού επιφανειακού στρώματος CuO. Δεξιά:
Διαβίβαση CO προκαλεί άμεση αναγωγή του επιφανειακού οξειδίου
προς αστραφτερό μεταλλικό χαλκό. (Φωτογραφίες από μια ωραία
σειρά σχετικώς ακίνδυνων και απλών πειραμάτων με CO που περιγράφονται στην
[Αναφ. 4γ])
|
 |
|
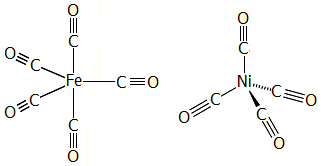
Τα τυπικότερα
παραδείγματα καρβονυλικών συμπλόκων: Αριστερά:
Πεντακαρβονυλικός σίδηρος(0), κιτρινωπό τοξικό υγρό δυσώδους
οσμής, σ.ζ. 103ºC. Χρησιμοποιήθηκε ως αντικροτικό καυσίμων
αυτοκινήτων. Δεξιά:
Τετρακαρβονυλικό νικέλιο(0), σχεδόν άχρωμο πτητικό και
ιδιαίτερα τοξικό υγρό
δυσώδους οσμής, σ.ζ. 43ºC. Ενδιάμεση ένωση στη βιομηχανική παρασκευή
καθαρού νικελίου (μέθοδος
Mond). |
|
 |
 |
|
Αριστερά:
Σφαιρίδια καθαρού νικελίου.
Δεξιά:
Ludwig Mond (1839-1909).
Βρετανός (γερμανικής καταγωγής)
χημικός και βιομήχανος. Γνωστός για την ομώνυμη μέθοδο
καθαρισμού του νικελίου. |
Πολλαπλασιαστικό
σύστημα CO2/CO
[Αναφ. 6]
Ενδιαφέρον ως ιδέα παρουσιάζει η ενισχυόμενη ή
πολλαπλασιαστική αντίδραση (amplification
reaction), που μπορεί να
χρησιμοποιηθεί για τoν πολλαπλασιασμό μικρών ποσοτήτων CO2
σε
αδρανές αέριο (π.χ. Ν2).
Ο πολλαπλασιασμός της ποσότητας του CO2
πετυχαίνεται μέσω πολλαπλών διαδοχικών σταδίων
αναγωγών του προς CO (με διαβίβαση μέσω σωλήνα με
επιλευκοχρυσωμένο άνθρακα στους 900ºC) και επανοξείδωσης του CO προς CO2
(με διαβίβασή του
μέσω σωλήνα με οξείδιο του χαλκού στους 500ºC).
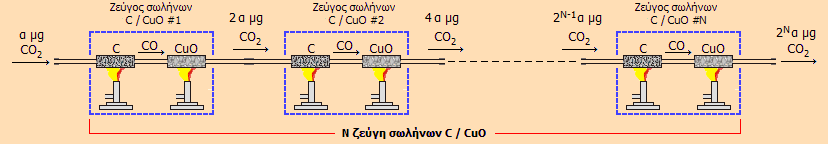
Κάθε "πέρασμα"
μιας ποσότητας CO2
μέσω ενός ζεύγους αυτών των δύο σωλήνων οδηγεί στον διπλασιασμό
της. 'Ετσι, πέρασμα μέσω δύο τέτοιων ζευγών
συνεπάγεται τετραπλασιασμό, μέσω τριών τέτοιων ζευγών
συνεπάγεται οκταπλασιασμό κ.ο.κ.
Η όλη διαδικασία μπορεί να θεωρηθεί ως "πρόγονος" των ευρύτατα
χρησιμοποιούμενων πλέον σύγχρονων τεχνικών πολλαπλασιασμού
τμημάτων DNA (τεχνική
PCR).
Το σύστημα δοκιμάστηκε με επιτυχία με μια σειρά 4 ζευγών
C/CuO, που θεωρητικά για κάθε
1 mg εισερχόμενου
CO2
παρέχει στην έξοδό της 16 mg CO2.
Η αλληλουχία των αντιδράσεων και μια σχηματική παράσταση ενός
τέτοιου "πολλαπλασιαστικού" συστήματος δείχνεται παρακάτω:

|
 |
|
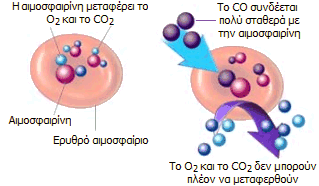
Η αιμοσφαιρίνη,
που βρίσκεται στα ερυθρά αιμοσφαίρια, μεταφέρει το Ο2
από τους πνεύμονες προς τους
ιστούς και από εκεί παραλαμβάνει το
CO2,
ως προϊόν των βιοχημικών "καύσεων" και το μεταφέρει προς τους
πνεύμονες, απ' όπου αποβάλλεται με την εκπνοή. Οι συνδέσεις του
O2
και του
CO2
με την
αιμοσφαιρίνη είναι "χαλαρές". Το CO
συνδέεται "σταθερά" με την αιμοσφαιρίνη στερώντας της την ικανότητα
να μεταφέρει το Ο2
και το CO2. |
|
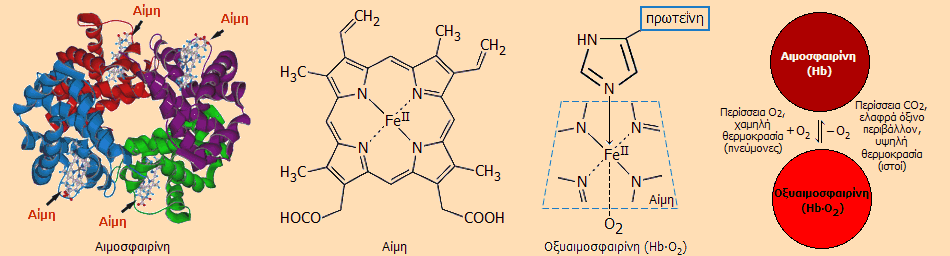
Σύνδεση
αιμοσφαιρίνης με το Ο2 και το CO
[Αναφ.
8]
Η
αιμοσφαιρίνη (hemoglobin, Hb) είναι σιδηρούχος μεταλλοπρωτεΐνη και
αποτελεί σχεδόν το σύνολο της μάζας (97%) του ξηρού περιεχομένου
των ερυθρών αιμοσφαιρίων και το 35% της συνολικής μάζας τους. Το
μοριακό βάρος της είναι περίπου 64 kDa. Η αιμοσφαιρίνη δρα στον
οργανισμό ως "αντιστρεπτός φορέας οξυγόνου". 'Ενας
ενήλικας σε κατάσταση ηρεμίας καταναλίσκει περίπου 250 mL Ο2
το λεπτό. Η ποσότητα αυτή αυξάνεται δραματικά αν ο άνθρωπος
ασκεί μια έντονη σωματική προσπάθεια. Σχεδόν στο σύνολό του το
οξυγόνο μεταφέρεται στους ιστούς μέσω της αιμοσφαιρίνης. 'Εχει βρεθεί ότι 1 g
αιμοσφαιρίνης δεσμεύει 1,34 mL Ο2,
γεγονός που καθιστά το αίμα κατά 70 φορές πλουσιότερο σε οξυγόνο
απ' όσο θα ήταν απουσία της (δηλ. σε σχέση με το διαλυμένο
οξυγόνο). Η περιεκτικότητα του αίματος σε αιμοσφαιρίνη (σε g/dL)
είναι: 'Αντρες 13,5-16,5, γυναίκες 12,1-15,1, παιδιά 11-16 και
έγκυοι γυναίκες 11-12.
Η αιμοσφαιρίνη διαθέτει τέσσερις πρόσθετες ομάδες
αίμης (heme). Η
αίμη είναι ένα σύμπλοκο του Fe(II) με ένα παράγωγο της
πορφυρίνης.
Η αίμη συνδέεται μέσω του Fe(II) με το άζωτο του ιμιδαζολικού δακτυλίου μιας
ιστιδίνης (αμινοξύ) που αποτελεί τον σύνδεσμο με το υπόλοιπο πρωτεϊνικό τμήμα της αιμοσφαιρίνης. Το σύμπλοκο αυτό
προσδίδει το σκούρο κόκκινο χρώμα στην αιμοσφαιρίνη, όπως και την
ικανότητα να συνδέεται "χαλαρά" με το μοριακό οξυγόνο
(Ο2) μέσω του Fe(II) σχηματίζοντας οξυαιμοσφαιρίνη (oxyhemoglobulin) με
λαμπρό κόκκινο χρώμα.
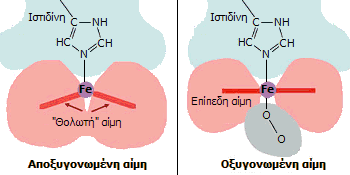 Δέσμευση Ο2.
Στην ελεύθερη αιμοσφαιρίνη (μη οξυγονωμένη) ο Fe(II) έλκεται
προς το άκρο της ιστιδίνης και η αίμη αποκτά ένα θολωτό σχήμα.
Ωστόσο, μόλις μία μονάδα αίμης συνδεθεί με το οξυγόνο, η αίμη
αποκτά πλήρως επίπεδο σχήμα. Αυτό προκαλεί μια έλξη της
ιστιδίνης (που δρα σαν ένα είδος μοριακής "σκανδάλης" ) προς το
επίπεδο της αίμης, γεγονός το οποίο προκαλεί μια σειρά αλλαγών
στη διαμόρφωση του μορίου της αιμοσφαιρίνης. Το τελικό
αποτέλεσμα αυτών των αλλαγών είναι η ακόμη ευκολότερη σύνδεση
των υπόλοιπων τριών μονάδων αίμης με μόρια οξυγόνου, μια
ιδιότητα της αιμοσφαιρίνης γνωστή ως συνεργατική σύνδεση
(cooperative binding). Δέσμευση Ο2.
Στην ελεύθερη αιμοσφαιρίνη (μη οξυγονωμένη) ο Fe(II) έλκεται
προς το άκρο της ιστιδίνης και η αίμη αποκτά ένα θολωτό σχήμα.
Ωστόσο, μόλις μία μονάδα αίμης συνδεθεί με το οξυγόνο, η αίμη
αποκτά πλήρως επίπεδο σχήμα. Αυτό προκαλεί μια έλξη της
ιστιδίνης (που δρα σαν ένα είδος μοριακής "σκανδάλης" ) προς το
επίπεδο της αίμης, γεγονός το οποίο προκαλεί μια σειρά αλλαγών
στη διαμόρφωση του μορίου της αιμοσφαιρίνης. Το τελικό
αποτέλεσμα αυτών των αλλαγών είναι η ακόμη ευκολότερη σύνδεση
των υπόλοιπων τριών μονάδων αίμης με μόρια οξυγόνου, μια
ιδιότητα της αιμοσφαιρίνης γνωστή ως συνεργατική σύνδεση
(cooperative binding).
Αποδέσμευση Ο2. Παρουσία CO2,
σε κάπως πιο όξινο pH και σε πιο θερμό
περιβάλλον (δηλ. στους ιστούς) το δεσμευμένο Ο2
αποσπάται από την οξυαιμοσφαιρίνη, εξαιτίας μιας μερικής
πρωτονίωσης της ιστιδίνης (φαινόμενο
Bohr). Εκτός από το
οξυγόνο, η αιμοσφαιρίνη συνδέεται χαλαρά, όμως μέσω ελεύθερων
αμινομάδων αμινοξέων του
πρωτεϊνικού της τμήματος με το διοξείδιο του άνθρακα
σχηματίζοντας καρβαμιδική ομάδα:
R- NH2
+ CO2
 R- NH-COO- + H+
R- NH-COO- + H+
Με ανάλογους τρόπους η αιμοσφαιρίνη και άλλα αέρια (π.χ. NO).
Δέσμευση CO και τα αποτελέσματά της. Σε περίπτωση εισπνοής
μονοξειδίου του άνθρακα, το αέριο δεσμεύεται (στη θέση του
O2)
σε μια μονάδα αίμης και
το γεγονός αυτό έχει ως αποτέλεσμα την ισχυρότερη δέσμευση του οξυγόνου
από τις άλλες τρεις ομάδες, οπότε δεν μπορεί να
αποδοθεί στους ιστούς. Στην ισχυρή αυτή δέσμευση του οξυγόνου
οφείλεται το έντονο ερυθρό χρώμα του αίματος των θυμάτων
δηλητηρίασης από CO.
Μέτρηση O2
στο αίμα.
Η μέτρηση του βαθμού οξυγόνωσης του αίματος είναι πλέον μια πολύ
απλή και μη επεμβατική διαδικασία. Η ελαφριά
διαφοροποίηση στο χρώμα του αίματος ανάλογα με την
περιεκτικότητά του σε οξυγονωμένη αιμοσφαιρίνη επιτρέπει την εύκολη και συνεχή
φωτομετρική μέτρηση του κορεσμού του αίματος σε O2
(sPO2%,
ποσοστό οξυαιμοσφαιρίνης Hb O2
ως προς την ολική αιμοσφαιρίνης). Επίσης, επιτρέπει τη μέτρηση
του αντίστοιχου ποσοστού καρβοξυαιμοσφαιρίνης (Hb O2
ως προς την ολική αιμοσφαιρίνης). Επίσης, επιτρέπει τη μέτρηση
του αντίστοιχου ποσοστού καρβοξυαιμοσφαιρίνης (Hb CO)
στις περιπτώσεις δηλητηρίασης με CO. Η μέτρηση του κορεσμού του
αίματος σε O2
έχει ιδιαίτερη κλινική σημασία και δείχνει το πόσο καλά
οξυγονώνεται ο οργανισμός και παρίσταται ανάγκη χορήγησης
καθαρού οξυγόνου. Οι μονάδες
αυτές, γνωστές ως
οξύμετρα (oxymeters) βρίσκονται δίπλα
στους ασθενείς σε κάθε μονάδα εντατικής θεραπείας. CO)
στις περιπτώσεις δηλητηρίασης με CO. Η μέτρηση του κορεσμού του
αίματος σε O2
έχει ιδιαίτερη κλινική σημασία και δείχνει το πόσο καλά
οξυγονώνεται ο οργανισμός και παρίσταται ανάγκη χορήγησης
καθαρού οξυγόνου. Οι μονάδες
αυτές, γνωστές ως
οξύμετρα (oxymeters) βρίσκονται δίπλα
στους ασθενείς σε κάθε μονάδα εντατικής θεραπείας.
|
 |
 |
 |
|
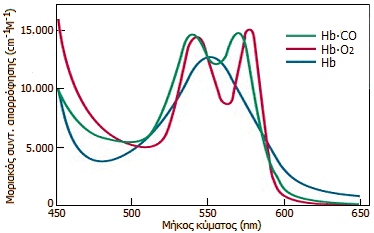
Αριστερά:
Φάσματα απορρόφησης (στο ορατό) της ελεύθερης
αιμοσφαιρίνης, της οξυαιμοσφαιρίνης και της
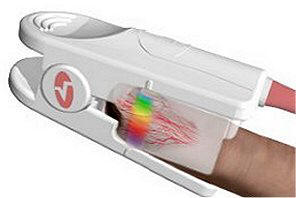
καρβοξυαιμοσφαιρίνης. Μέσο: Φορητή
μονάδα συνεχούς μέτρησης του κορεσμού Ο2
της αιμοσφαιρίνης, όπως και του ποσοστού Hb CO
(Παλμικό οξύμετρο
Rad-57 TM Pulse CO-Oximeter, Masimo Corporation,
Irving, CA). Δεξιά: Η μέτρηση πετυχαίνεται με
φωτομετρικές μετρήσεις σε δύο διαφορετικά μήκη κύματος:
στα 660 nm στο ορατό και στα 940 nm του εγγύς
υπέρυθρου (NIR) με έναν αισθητήρα που τοποθετείται στο
δάκτυλο του ασθενούς. Στον αισθητήρα είναι
ενσωματωμένες τόσο οι πηγές φωτός (LED) όσο και οι
ανιχνευτές (οπτοτρανζίστορ)
[Αναφ.
8γ]. Με διαδοχικές μετρήσεις
στα δύο μήκη κύματος κατά τη διάρκεια του σφυγμικού
κύματος και με κατάλληλη μαθηματική επεξεργασία των
λαμβανόμενων σημάτων (με τη βοήθεια του ενσωματωμένου
στο οξύμετρο μικροεπεξεργαστή) υπολογίζεται και
παρουσιάζεται σε ψηφιακή ένδειξη αυτόματα ο
βαθμός κορεσμού του αίματος σε Ο2.
Ανάλογα, μετρείται και το ποσοστό Hb CO
(Παλμικό οξύμετρο
Rad-57 TM Pulse CO-Oximeter, Masimo Corporation,
Irving, CA). Δεξιά: Η μέτρηση πετυχαίνεται με
φωτομετρικές μετρήσεις σε δύο διαφορετικά μήκη κύματος:
στα 660 nm στο ορατό και στα 940 nm του εγγύς
υπέρυθρου (NIR) με έναν αισθητήρα που τοποθετείται στο
δάκτυλο του ασθενούς. Στον αισθητήρα είναι
ενσωματωμένες τόσο οι πηγές φωτός (LED) όσο και οι
ανιχνευτές (οπτοτρανζίστορ)
[Αναφ.
8γ]. Με διαδοχικές μετρήσεις
στα δύο μήκη κύματος κατά τη διάρκεια του σφυγμικού
κύματος και με κατάλληλη μαθηματική επεξεργασία των
λαμβανόμενων σημάτων (με τη βοήθεια του ενσωματωμένου
στο οξύμετρο μικροεπεξεργαστή) υπολογίζεται και
παρουσιάζεται σε ψηφιακή ένδειξη αυτόματα ο
βαθμός κορεσμού του αίματος σε Ο2.
Ανάλογα, μετρείται και το ποσοστό Hb CO
το οποίο είναι γραμμική συνάρτηση του λόγου
των απορροφήσεων στα μήκη κύματος 541 nm
και 555 nm
[Αναφ. 7β]. CO
το οποίο είναι γραμμική συνάρτηση του λόγου
των απορροφήσεων στα μήκη κύματος 541 nm
και 555 nm
[Αναφ. 7β]. |
|
|
Ηλεκτρονικοί
ανιχνευτές CO [Αναφ. 9]
Η
εγκατάσταση ηλεκτρονικών ανιχνευτών μονοξειδίου του άνθρακα στα σπίτια τα
οποία
θερμαίνονται με τζάκια, σόμπες και αλλά αυτόνομα συστήματα θέρμανσης, που
βασίζονται στην καύση οργανικών υλικών (καύσιμα, ξύλα, pellets) μπορεί να
σώσει ζωές και είναι 100% απαραίτητη.
Σε πολλές χώρες η εγκατάσταση ανιχνευτών CO ήδη είναι υποχρεωτική.
Οι συσκευές αυτές είναι φθηνές (τυπικές τιμές αρχίζουν από 20 ευρώ περίπου)
και μπορούν να βρεθούν εύκολα στην αγορά.
Ακριβότεροι είναι οι μετρητές
βιομηχανικών εγκαταστάσεων που πέραν από ηχητικό σήμα προειδοποίησης
παρέχουν και ενδείξεις της περιεκτικότητας του αέρα σε CO. Τη δυνατότητα
αυτή έχουν και ορισμένοι από τους ακριβότερους οικιακούς ανιχνευτές.
Οι παραπάνω ανιχνευτές κάνουν χρήση αισθητήρων CO
διαφόρων τύπων, όπως είναι οι ηλεκτροχημικοί, οι
ημιαγωγοί και οι βιομιμητικοί αισθητήρες.
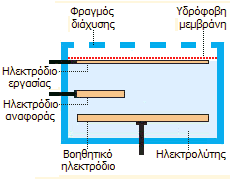
Οι ηλεκτροχημικοί
αισθητήρες CO (αμπερομετρικοί αισθητήρες)
βασίζονται στη μέτρηση του ρεύματος ηλεκτρολυτικού στοιχείου όπου στην ποτενσιοστατούμενη άνοδο οξειδώνεται (σε διάλυμα H2SO4)
το CO προς CO2,
ενώ στην κάθοδο ανάγεται το Ο2
προς Η2Ο,
σύμφωνα με τις ηλεκτροδιακές αντιδράσεις:
'Ανοδος : CO + H2O
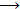 CO2 + 2H+ + 2e-
Κάθοδος: Ο2 + 4Η+
+ 4e- CO2 + 2H+ + 2e-
Κάθοδος: Ο2 + 4Η+
+ 4e-
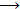 2Η2Ο
2Η2Ο
Η άνοδος (ηλεκτρόδιο εργασίας) βρίσκεται σε επαφή με
τον εξεταζόμενο χώρο μέσω πορώδους υδρόφοβου διαφράγματος, το οποίο επιτρέπει την είσοδο
μορίων του αερίου CO, όχι όμως τη διαρροή του ηλεκτρολυτικού διαλύματος. Οι
αισθητήρες αυτοί διαθέτουν μεγάλη "γραμμική περιοχή", μεγάλη ευαισθησία,
αλλά το κόστος τους είναι σχετικά μεγάλο. Επιπλέον, απαιτούν τακτική (π.χ.
κάθε 1 ή 2 χρόνια) αντικατάσταση και είναι καταλληλότεροι για
βιομηχανικούς σκοπούς.
Οι ημιαγωγοί αισθητήρες
(ή αισθητήρες στερεάς κατάστασης) βασίζονται στην επίδραση του CO στην αγωγιμότητα (σε υψηλή θερμοκρασία (400ºC) νηματίων SnO2.
Η αγωγιμότητα του υλικού αυτού αυξάνεται παρουσία CO, ενώ μειώνεται παρουσία O2.
Μειονέκτημα αυτών των ανιχνευτών CO είναι το ότι λόγω της
απαιτούμενης υψηλής θερμοκρασίας, είναι η αδύνατη λειτουργία τους με
μπαταρίες, αλλά απαιτούν συνεχή τροφοδοσία μέσω της ηλεκτρικής εγκατάστασης
του χώρου που ελέγχουν.
Οι βιομιμητικοί αισθητήρες
βασίζονται στη φωτομετρική παρακολούθηση της ελαφριάς αλλαγής του χρώματος
ζελέ αιμοσφαιρίνης ή ενός συνθετικού αναλόγου (γίνεται λίγο πιο σκούρο
παρουσία CO) και αποτελούν τους απλούστερους τύπους ανιχνευτών CO. Ο χρόνος
απόκρισής τους είναι σχετικά μεγάλος και εξαρτάται από τη συγκέντρωση CO στον
αέρα. Τυπικά, οι ανιχνευτές που χρησιμοποιούν βιομιμητικούς αισθητήρες για συγκέντρωση CO 70 ppm παρέχουν σήμα μετά από 1 ώρα, ενώ για
συγκέντρωση CO 400 ppm παρέχουν σήμα σε 4 λεπτά. Ωστόσο, αυτό δεν αποτελεί
σοβαρό μειονέκτημα και οι βιομιμητικοί ανιχνευτές αποτελούν τον
φθηνότερο και συνηθέστερα χρησιμοποιούμενο τύπο ανιχνευτή CO για τα σπίτια.
|
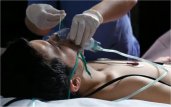
Τα συμπτώματα της
δηλητηρίασης από το CO εξαρτώνται από το ποσοστό της αιμοσφαιρίνης που
έχει δεσμευτεί από το CO ως καρβοξυαιμοσφαιρίνη (Hb CO). Κατά την
εισπνοή αέρα που περιέχει CO, η τιμή % Hb CO). Κατά την
εισπνοή αέρα που περιέχει CO, η τιμή % Hb CO αυξάνει μέχρις ότου
φτάσει σε μια τιμή ισορροπίας που εξαρτάται από τη συγκέντρωση CO στον
αέρα. Στο διάγραμμα δεξιά δείχνεται πως μεταβάλλεται η τιμή % Hb CO αυξάνει μέχρις ότου
φτάσει σε μια τιμή ισορροπίας που εξαρτάται από τη συγκέντρωση CO στον
αέρα. Στο διάγραμμα δεξιά δείχνεται πως μεταβάλλεται η τιμή % Hb CO
ως προς το χρόνο σε τρία επίπεδα συγκέντρωσης CO (με τα μπλε σημεία
αποδίδονται οι πειραματικές τιμές, ενώ με κόκκινες καμπύλες
γραμμές αποδίδονται οι θεωρητικές τιμές με βάση ένα προτεινόμενο μαθηματικό
μοντέλο, [Αναφ. 7δ]). 'Ετσι, από
το διάγραμμα αυτό σε συνδυασμό με τον προηγούμενο πίνακα συμπτωμάτων
προκύπτουν τα εξής συμπεράσματα: Μετά από περίπου 30 ώρες εισπνοής
αέρα μολυσμένου με 25 ppm CO, η Hb CO
ως προς το χρόνο σε τρία επίπεδα συγκέντρωσης CO (με τα μπλε σημεία
αποδίδονται οι πειραματικές τιμές, ενώ με κόκκινες καμπύλες
γραμμές αποδίδονται οι θεωρητικές τιμές με βάση ένα προτεινόμενο μαθηματικό
μοντέλο, [Αναφ. 7δ]). 'Ετσι, από
το διάγραμμα αυτό σε συνδυασμό με τον προηγούμενο πίνακα συμπτωμάτων
προκύπτουν τα εξής συμπεράσματα: Μετά από περίπου 30 ώρες εισπνοής
αέρα μολυσμένου με 25 ppm CO, η Hb CO σταθεροποιείται περίπου στο
3-4%, επίπεδο στο οποίο δεν παρατηρούνται κάποια συμπτώματα. Μετά από 15 ώρες
εισπνοής αέρα μολυσμένο με 200 ppm CO, η Hb CO σταθεροποιείται περίπου στο
3-4%, επίπεδο στο οποίο δεν παρατηρούνται κάποια συμπτώματα. Μετά από 15 ώρες
εισπνοής αέρα μολυσμένο με 200 ppm CO, η Hb CO προβλέπεται να σταθεροποιηθεί περίπου στο 30%,
οπότε αναμένεται ως σύμπτωμα ένας έντονος πονοκέφαλος ίσως και ναυτία,
ενώ εισπνοή αέρα μολυσμένου με 1000 ppm CO, προβλέπεται ότι μέσα σε 2-3 ώρες η Hb CO προβλέπεται να σταθεροποιηθεί περίπου στο 30%,
οπότε αναμένεται ως σύμπτωμα ένας έντονος πονοκέφαλος ίσως και ναυτία,
ενώ εισπνοή αέρα μολυσμένου με 1000 ppm CO, προβλέπεται ότι μέσα σε 2-3 ώρες η Hb CO θα έχει
φτάσει σε εξαιρετικώς επικίνδυνα επίπεδα (>50-60%) που οδηγούν σε κώμα,
μόνιμες εγκεφαλικές βλάβες και τελικά στον θάνατο. CO θα έχει
φτάσει σε εξαιρετικώς επικίνδυνα επίπεδα (>50-60%) που οδηγούν σε κώμα,
μόνιμες εγκεφαλικές βλάβες και τελικά στον θάνατο. |
 |
|
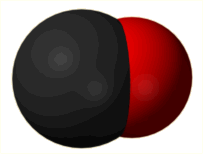
Μόνο με αυτόνομες
αναπνευστικές συσκευές μπορεί να εισέλθει κανείς σε χώρους με
τοξικά επίπεδα μονοξειδίου του άνθρακα.
Οι απλές μάσκες με φίλτρα είναι τελείως ανεπαρκείς. |
|

Στους καπνιστές τό
επίπεδο καρβοξυαιμοσφαιρίνης μπορεί να φτάσει το 15%. Το επίπεδο
αυτό αντιστοιχεί με το να ζει κανείς σε σε μια ατμόσφαιρα που
περιέχει μόνιμα μια συγκέντρωση CO περίπου 100 ppm.
|
Χρήση του
μονοξειδίου του άνθρακα στην Ιατρική ;
[Αναφ. 12]
Σχετικά πρόσφατες έρευνες έδειξαν ότι το
μονοξείδιο του άνθρακα δεν είναι και τόσο "αφύσικη" ουσία για τον ανθρώπινο
οργανισμό. Μικροποσότητες
CO παράγονται φυσιολογικά στο ανθρώπινο
σώμα ως αποτέλεσμα οξειδωτικής δράσης ορισμένων ενζύμων (οξυγενάσες) στην αίμη, που προέρχεται από τη διάσπαση
της αιμοσφαιρίνης. 'Ετσι δικαιολογείται η παρουσία μικρών ποσοτήτων καρβοξυαιμοσφαιρίνης ακόμη και σε άτομα που δεν είχαν εκτεθεί σε μονοξείδιο του
άνθρακα.
Το 1993
διαπιστώθηκε ότι το CO
(μαζί με τα αέρια
NO και H2S) δρα ως
νευροδιαβιβαστής
(neurotransmitter) και σχηματίζεται ως αποτέλεσμα
φυσιολογικής απόκρισης του οργανισμού σε φλεγμονές. Από τότε
αποτέλεσε αντικείμενο έρευνας ως προς τον βιολογικό του ρόλο. Και τα τρία αέρια
είναι σήμερα γνωστό ότι ασκούν αγγειοδιασταλτική δράση και ότι υποβοηθούν την αγγειογένεση στις περιπτώσεις φλεγμονών. Ωστόσο, η αγγειογένεση δεν είναι
πάντοτε επιθυμητή, ιδιαίτερα στις περιπτώσεις κακοήθων όγκων, αφού βοηθά την
τροφοδοσία και την ανάπτυξή τους, όπως επίσης θεωρείται επιβαρυντική στις
περιπτώσεις εκφύλισης της ωχράς κηλίδας.
|

Και τα δύο
κρέατα είναι εξίσου φρέσκα. Ωστόσο, το αριστερό υπέστη
επεξεργασία με CO (πηγή). |
Σήμερα, σε πολλά
εργαστήρια πραγματοποιούνται μελέτες πάνω στη αντιφλεγμονώδη και
κυτταροπροστατευτική δράση του CO. Αυτές οι ιδιότητες
του CO ενδεχομένως μπορούν να χρησιμοποιηθούν για
την πρόληψη μιας σειράς παθολογικών καταστάσεων, όπως είναι η
βλαβη επαναιμάτωσης (ischemia
reperfusion injury) κατά την αποκατάσταση της κυκλοφορίας του αίματος
μετά από ισχαιμικά επεισόδια, η απόρριψη μοσχευμάτων, η
αρτηριοσκλήρυνση, σοβαρά σηπτικά
επεισόδια, σοβαρές περιπτώσεις ελονοσίας και διάφορα αυτοάνοσα νοσήματα. 'Εχουν
διεξαχθεί πειράματα σε ανθρώπους αλλά ακόμη δεν είναι γνωστά τα
αποτελέσματα.
Μια λιγότερο γνωστή εφαρμογή του μονοξειδίου
του άνθρακα [Αναφ. 13]
Το μονοξείδιο του άνθρακα χρησιμοποιείται ως
υλικό συσκευασίας "τροποποιημένης ατμόσφαιρας" στις ΗΠΑ για φρέσκα κρέατα
(βοδινό, χοιρινό) και ψάρια. Απλά, τα κάνει να φαίνονται πιο φρέσκα απ' ό,τι
μπορεί να είναι. Το CO συνδέεται με τη
μυοσφαιρίνη τους και παρέχει καρβοξυμυοσφαιρίνη η οποία προσδίδει στο κρέας ένα λαμπρό κερασέρυθρο χρώμα. Για να αναπτυχθεί αυτό το χρώμα αρκεί μια
περιεκτικότητα της ατμόσφαιρας σε CO 0,4 έως 0,5%.Το χρώμα αυτό διατηρείται πολύ περισσότερο απ' όσο στα
κρέατα που συσκευάζονται στην κανονική ατμόσφαιρα.
Αν και το 2002 η τεχνολογία αυτή χαρακτηρίστηκε
από την Διεύθυνση Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) ως GRAS (generally recognized as safe: "γενικά
αναγνωριζόμενη ως
ασφαλής"), υπήρξαν δικαιολογημένοι φόβοι ότι η πρακτική αυτή θα μπορούσε να καλύψει τυχόν
αλλοιώσεις του κρέατος. 'Ετσι, ζητήθηκε να αναγράφεται η χρήση αυτή του CO στην ετικέτα
του τροφίμου και
να θεωρηθεί το CO ως χρωστικό πρόσθετο. Ωστόσο, το θέμα αυτό αυτό δεν
φαίνεται να προχώρησε. Θα πρέπει να σημειωθεί ότι η χρήση αυτή του
μονοξειδίου του άνθρακα για τον σκοπό αυτό απαγορεύεται σε πολλές χώρες, όπως στον Καναδά, στην
Ιαπωνία και στην Ευρωπαϊκή 'Ενωση.
Ορισμένα
από τα πολλά βιβλία τα οποία έχουν κυκλοφορήσει για το
μονοξείδιο του άνθρακα που κυρίως αναφέρονται
στην τοξικότητά του και τα
ενδεικνυόμενα μέτρα ασφάλειας (από: Amazon.com και
Google-books).
13.
(α)
Deryck Damian Pattron DD: "Carbon
Monoxide Packaging of Meats May Mask Spoilage & Compromise Public Health
Safety", Internet
Journal of Food Safety 9:49-51,
2007 (αρχείο
PDF, 40 ΚΒ). (β)
Weiss R: "FDA
Is Urged to Ban Carbon-Monoxide-Treated Meat", Washington Post Staff,
February 20, 2006. (γ) Schmit J: "Carbon
monoxide keeps meat red longer; is that good?", USA TODAY, October 30,
2007. (δ)
American Meat
Institute: "Carbon
Monoxide in Meat Packaging: Myths and Facts"
2008 (αρχείο
PDF, 141 KB).










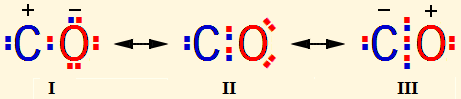
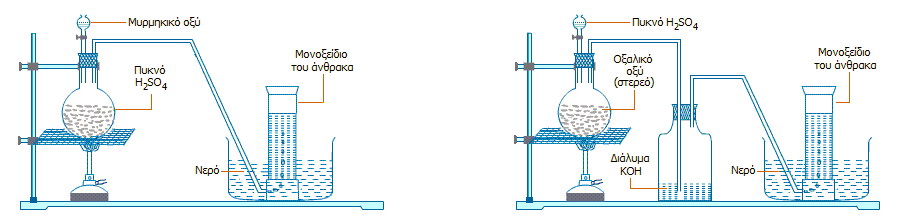
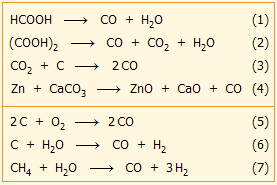 Εργαστηριακές
παρασκευές. Σε εργαστηριακή κλίμακα CO παρασκευάζεται πολύ εύκολα
και με μεγάλο βαθμό καθαρότητας με αφυδάτωση του μυρμηκικού οξέος ή του
οξαλικού οξέος με
πυκνό-θερμό θειικό οξύ ή με
Εργαστηριακές
παρασκευές. Σε εργαστηριακή κλίμακα CO παρασκευάζεται πολύ εύκολα
και με μεγάλο βαθμό καθαρότητας με αφυδάτωση του μυρμηκικού οξέος ή του
οξαλικού οξέος με
πυκνό-θερμό θειικό οξύ ή με 




 Το
μονοξείδιο του άνθρακα είναι μια σταθερότατη χημική ένωση και μόνο σε πολύ υψηλές θερμοκρασίες
(>2000
Το
μονοξείδιο του άνθρακα είναι μια σταθερότατη χημική ένωση και μόνο σε πολύ υψηλές θερμοκρασίες
(>2000 Το CO σε υψηλές θερμοκρασίες είναι ισχυρό
αναγωγικό μέσο και παρέχει μεγάλο αριθμό χαρακτηριστικών αντιδράσεων
αναγωγής. 'Ετσι, χρησιμοποιείται στη μεταλλουργία για την αναγωγή πολλών
μεταλλικών οξειδίων προς μέταλλα (αντιδράσεις 14-16).
Το CO σε υψηλές θερμοκρασίες είναι ισχυρό
αναγωγικό μέσο και παρέχει μεγάλο αριθμό χαρακτηριστικών αντιδράσεων
αναγωγής. 'Ετσι, χρησιμοποιείται στη μεταλλουργία για την αναγωγή πολλών
μεταλλικών οξειδίων προς μέταλλα (αντιδράσεις 14-16). 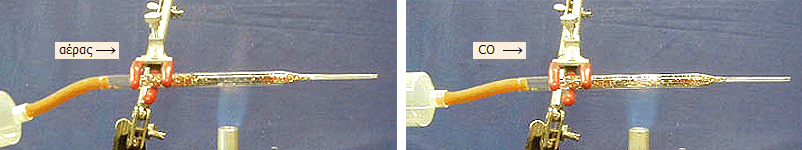



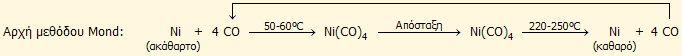

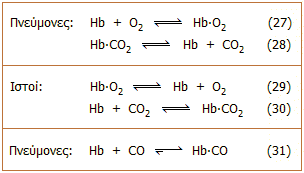


 Δέσμευση Ο2.
Στην ελεύθερη αιμοσφαιρίνη (μη οξυγονωμένη) ο Fe(II) έλκεται
προς το άκρο της ιστιδίνης και η αίμη αποκτά ένα θολωτό σχήμα.
Ωστόσο, μόλις μία μονάδα αίμης συνδεθεί με το οξυγόνο, η αίμη
αποκτά πλήρως επίπεδο σχήμα. Αυτό προκαλεί μια έλξη της
ιστιδίνης (που δρα σαν ένα είδος μοριακής "σκανδάλης" ) προς το
επίπεδο της αίμης, γεγονός το οποίο προκαλεί μια σειρά αλλαγών
στη διαμόρφωση του μορίου της αιμοσφαιρίνης. Το τελικό
αποτέλεσμα αυτών των αλλαγών είναι η ακόμη ευκολότερη σύνδεση
των υπόλοιπων τριών μονάδων αίμης με μόρια οξυγόνου, μια
ιδιότητα της αιμοσφαιρίνης γνωστή ως συνεργατική σύνδεση
(cooperative binding).
Δέσμευση Ο2.
Στην ελεύθερη αιμοσφαιρίνη (μη οξυγονωμένη) ο Fe(II) έλκεται
προς το άκρο της ιστιδίνης και η αίμη αποκτά ένα θολωτό σχήμα.
Ωστόσο, μόλις μία μονάδα αίμης συνδεθεί με το οξυγόνο, η αίμη
αποκτά πλήρως επίπεδο σχήμα. Αυτό προκαλεί μια έλξη της
ιστιδίνης (που δρα σαν ένα είδος μοριακής "σκανδάλης" ) προς το
επίπεδο της αίμης, γεγονός το οποίο προκαλεί μια σειρά αλλαγών
στη διαμόρφωση του μορίου της αιμοσφαιρίνης. Το τελικό
αποτέλεσμα αυτών των αλλαγών είναι η ακόμη ευκολότερη σύνδεση
των υπόλοιπων τριών μονάδων αίμης με μόρια οξυγόνου, μια
ιδιότητα της αιμοσφαιρίνης γνωστή ως συνεργατική σύνδεση
(cooperative binding).












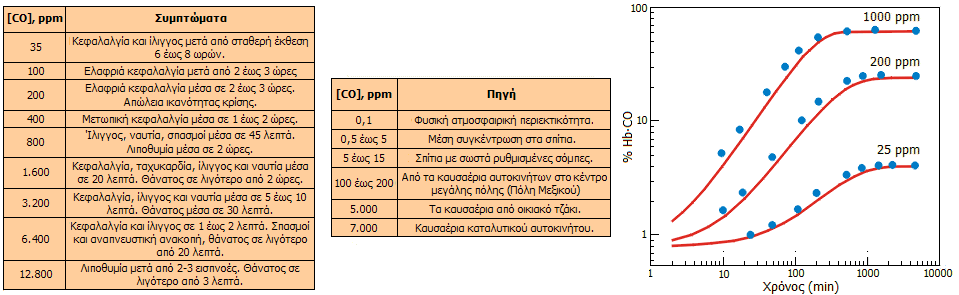
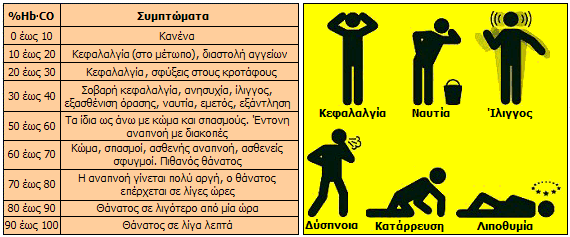 Συμπτώματα
της δηλητηρίασης από μονοξείδιο του άνθρακα.
Τα συμπτώματα της δηλητηρίασης
του ανθρώπου από το CO κατά σειρά εμφάνισής τους είναι: Κεφαλαλγία (πονοκέφαλος), ναυτία και ίλιγγος (ζάλη),
καταρροή, δύσπνοια, εξάντληση,
ταχυκαρδία, πόνος στο στήθος, λιποθυμία, θάνατος
από ασφυξία. Το πόσο γρήγορα διαδέχεται το ένα σύμπτωμα το άλλο, όπως και το αν τα
συμπτώματα φθάνουν μέχρι ένα δεδομένο επίπεδο ή αν τελικά οδηγούν στον θάνατο,
εξαρτάται από τη συγκέντρωση του CO στην ατμόσφαιρα και
φυσικά από τον χρόνο έκθεσης στην ατμόσφαιρα αυτή.
Συμπτώματα
της δηλητηρίασης από μονοξείδιο του άνθρακα.
Τα συμπτώματα της δηλητηρίασης
του ανθρώπου από το CO κατά σειρά εμφάνισής τους είναι: Κεφαλαλγία (πονοκέφαλος), ναυτία και ίλιγγος (ζάλη),
καταρροή, δύσπνοια, εξάντληση,
ταχυκαρδία, πόνος στο στήθος, λιποθυμία, θάνατος
από ασφυξία. Το πόσο γρήγορα διαδέχεται το ένα σύμπτωμα το άλλο, όπως και το αν τα
συμπτώματα φθάνουν μέχρι ένα δεδομένο επίπεδο ή αν τελικά οδηγούν στον θάνατο,
εξαρτάται από τη συγκέντρωση του CO στην ατμόσφαιρα και
φυσικά από τον χρόνο έκθεσης στην ατμόσφαιρα αυτή.