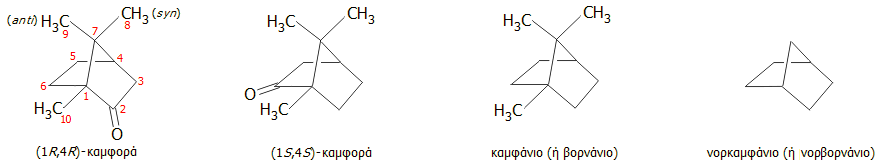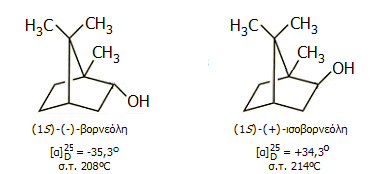Γενικά για τη καμφορά [Αναφ. 1]
 Η
καμφορά αποτελεί το κύριο συστατικό της ρητίνης
του
καμφορόδεντρου (Cinnamomum camphora),
ενός μεγάλων διαστάσεων αειθαλούς δέντρου, το
οποίο ανήκει στην οικογένεια των Δαφνοειδών
(Lauraceae). Το
καμφορόδεντρο (ή απλά "καμφορά") αναπτύσσεται σε
αμμώδη και ξηρά εδάφη και μπορεί να φθάσει τα 30 m ύψος και
ο κορμός του μπορεί να ξεπεράσει σε διάμετρο τα
5 m και είναι ενδημικό στη Νοτιοανατολική Ασία, στις Κίνα, Ιαπωνία,
Ταϊβάν και στην
Ινδονησία. Το δέντρο αυτό έχει καλλιεργηθεί με διάφορους
βαθμούς επιτυχίας στην Ινδία, Αίγυπτο,
Μαδαγασκάρη, νότια Ευρώπη, Καλιφόρνια και
Φλόριντα. 'Αφθονη καμφορά βρίσκεται και στη
ρητίνη του δέντρου-γίγαντα
Dryobalanops aromatica,
ενός είδους βελανιδιάς, που συναντάται στις
ζούγκλες της νήσου Βόρνεο.
Η
καμφορά αποτελεί το κύριο συστατικό της ρητίνης
του
καμφορόδεντρου (Cinnamomum camphora),
ενός μεγάλων διαστάσεων αειθαλούς δέντρου, το
οποίο ανήκει στην οικογένεια των Δαφνοειδών
(Lauraceae). Το
καμφορόδεντρο (ή απλά "καμφορά") αναπτύσσεται σε
αμμώδη και ξηρά εδάφη και μπορεί να φθάσει τα 30 m ύψος και
ο κορμός του μπορεί να ξεπεράσει σε διάμετρο τα
5 m και είναι ενδημικό στη Νοτιοανατολική Ασία, στις Κίνα, Ιαπωνία,
Ταϊβάν και στην
Ινδονησία. Το δέντρο αυτό έχει καλλιεργηθεί με διάφορους
βαθμούς επιτυχίας στην Ινδία, Αίγυπτο,
Μαδαγασκάρη, νότια Ευρώπη, Καλιφόρνια και
Φλόριντα. 'Αφθονη καμφορά βρίσκεται και στη
ρητίνη του δέντρου-γίγαντα
Dryobalanops aromatica,
ενός είδους βελανιδιάς, που συναντάται στις
ζούγκλες της νήσου Βόρνεο.
 Καμφορά μαζί με άλλες
ανάλογες ενώσεις βρίσκεται στις ρητίνες και τα
αρωματικά έλαια πολλών φυτών, δέντρων και θάμνων της
ίδιας περιοχής, αλλά και της Αφρικής. Ο
βιολογικός ρόλος της είναι να δρα ως αμυντικό
μέσο των φυτικών οργανισμών κατά των διαφόρων
εντόμων.
Καμφορά μαζί με άλλες
ανάλογες ενώσεις βρίσκεται στις ρητίνες και τα
αρωματικά έλαια πολλών φυτών, δέντρων και θάμνων της
ίδιας περιοχής, αλλά και της Αφρικής. Ο
βιολογικός ρόλος της είναι να δρα ως αμυντικό
μέσο των φυτικών οργανισμών κατά των διαφόρων
εντόμων.
Οι αρχαίοι Αιγύπτιοι, όπως και οι κάτοικοι της Μεσοποταμίας χρησιμοποιούσαν το αρωματικό ξύλο και τη ρητίνη του καμφορόδεντρου για θυμιάματα σε θρησκευτικές τελετές, πολύ πριν η χρήση της ρητίνης του εξαπλωθεί στο αρχαίο Ελληνικό και Ρωμαϊκό κόσμο. Οι Αιγύπτιοι χρησιμοποιούσαν την πλούσια σε καμφορά ρητίνη του δέντρου, μαζί με άλλες ρητίνες και αιθέρια έλαια, για την ταρίχευση των νεκρών.
Από τις περιοχές των Ανατολικών Ινδιών (νοτιοανατολική Ασία) και μέσω των εμπορικών οδών που ήλεγχαν οι 'Αραβες, έφτασε (ξανά) η καμφορά στη μεσαιωνική Ευρώπη, μαζί με άλλες αρωματικές ρητίνες και σπάνια και πολύτιμα μπαχαρικά. Στις μουσουλμανικές χώρες χρησιμοποιούσαν την καμφορά ως μυρωδικό σε διάφορα εδέσματα. Μέχρι τον 18ο αιώνα, αποδίδονταν μαγικές και θεραπευτικές ιδιότητες στα διάφορα θυμιάματα και σε αυτά περιλαμβανόταν πάντοτε και η καμφορά.
Ιδιαίτερα διαδεδομένη ήταν η χρήση του αρωματικού ξύλου του καμφορόδεντρου στην Κίνα και πρώτος ανέφερε την ευρύτατη χρήση της καμφοράς στην Κίνα ο πασίγνωστος Ιταλός έμπορος-ταξιδευτής Marco Polo (1254-1324). Ο Βρετανός ιστορικός και γεωγράφος R. A. Donkin (1928-2006) αναφέρει σε βιβλίο του σχετικό με την ιστορία και τη γεωγραφία της καμφοράς, ότι το έτος 977, ο μαχαραγιάς της νήσου Βόρνεο έστειλε στον Κινέζο αυτοκράτορα, σε ένδειξη τιμής, τρία διαφορετικά είδη καμφοράς και πέντε φορτία πολύτιμου ξύλου καμφοράς (camphorwood). Ακόμη, μας πληροφορεί ότι οι Κινέζοι αξιωματούχοι δέχονταν ως δώρα και δωροδοκίες ποσότητες καμφοράς.
Την καμφορά στην Κίνα την ονόμαζαν άρωμα μυαλού δράκου (dragon's brain perfume), ονομασία που αποτελεί και τον τίτλο του σχετικού βιβλίου του Donkin. Στο βιβλίο αυτό αναφέρει ότι ένας Ισπανός ιεραπόστολος γύρω στο 1650 στην Κίνα είχε πληροφορηθεί, ότι στη νήσο Βόρνεο η καμφορά κυριολεκτικά ανάβλυζε από τον κορμό και τα κλαδιά κάποιων δέντρων σε άφθονες ποσότητες και οι ιθαγενείς τη συνέλεγαν σε υφάσματα που είχαν απλωμένα κάτω από το δέντρο αυτό, στα οποία έπεφτε σαν ημίρρευστη ρητίνη όπου και στερεοποιούνταν.
 |
 |
 |
| Το καμφορόδεντρο ή (απλά) καμφορά (Cinnamomum camphora), τα φύλλα και οι καρποί του. Αειθαλές δέντρο που φτάνει σε ύψος τα 20-30 m, ιθαγενές της ΝΑ Ασίας και διάμετρο κορμού τα 5 m. Τα φύλλα του έχουν μια κηρώδη υφή και έντονη οσμή καμφοράς. | Το δέντρο Dryobalanops aromatica της νήσου Βόρνεο, πηγή καμφοράς και καμφορόξυλου [πηγή]. | Αφρικανικός μπλε βασιλικός (african blue basil).Το αιθέριο έλαιό του περιέχει και μέχρι 22% καμφορά. [πηγή]. |
O Dokin αναφέρει ότι ο Παπικός Λεγάτος στην Αυλή του Μογγόλου κατακτητή Τζένγκις Χαν (1162-1227) επέστρεψε στην Ευρώπη με δώρα μεταξύ των οποίων περιλαμβανόταν και καμφορά. Η καμφορά χρησιμοποιήθηκε ευρύτατα για καπνισμούς κατά τη διάρκεια της μεγάλης επιδημίας βουβωνικής πανώλης, η οποία έμεινε γνωστή στην ιστορία ως ο μαύρος θάνατος (black death), Η επιδημία αυτή έπληξε ολόκληρη την Ευρώπη κατά το διάστημα 1347-1351 και σύμφωνα με διάφορες εκτιμήσεις εξόντωσε το 30% έως 50% του πληθυσμού της.
|
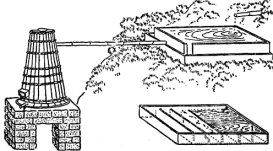
Ιαπωνικός αποστακτήρας καμφοράς [πηγή]. |
Κατά τον 17ο αιώνα η Ολλανδική Εταιρεία των Ανατολικών Ινδιών ήταν ο κύριος εισαγωγέας καμφοράς και εκτιμάται πως κάθε χρόνο έφερνε στην Ευρώπη περί τους 20-25 τόνους καμφοράς από τις αποθήκες της εταιρείας στο Μπαντάμ της νήσου Ιάβας.
Η ονομασία της καμφοράς προέρχεται από την αρχαία γαλλική camphre, η ίδια από τη μεσαιωνική λατινική camfora, αυτή από την αραβική λέξη kafur, η οποία με τη σειρά της προέρχεται από τη αρχαία μαλαϊκή kapur barus που σημαίνει "κιμωλία (chalk) του Barus", όπου το Barus είναι η ονομασία ενός αρχαίου λιμανιού της δυτικής ακτής της νήσου Σουμάτρα.
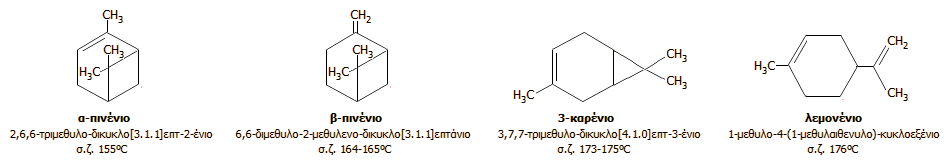
H καμφορά λαμβάνεται από το καμφορούχο υλικό (ξέσματα ξύλου κορμού, ρίζες, φύλλα, ρητίνη καμφορούχων δέντρων ή θάμνων) με απόσταξη με υδρατμούς και στη συνέχεια καθαρίζεται με εξάχνωση. Η ποσότητα καμφοράς που λαμβάνεται από το ξύλο του καμφορόδεντρου αποτελεί περίπου το 2-2,5% της μάζας του [Αναφ. 1δ]. Σήμερα οι μεγαλύτερες ποσότητες καμφοράς παρασκευάζονται πλέον ημισυνθετικά, με πρώτη ύλη το α-πινένιο (α-pinene), ένα από τα κύρια συστατικά (>50%) του τερεβινθελαίου (turpentine), του διαλύτη χρωμάτων που είναι ευρύτερα γνωστός ως "νέφτι".
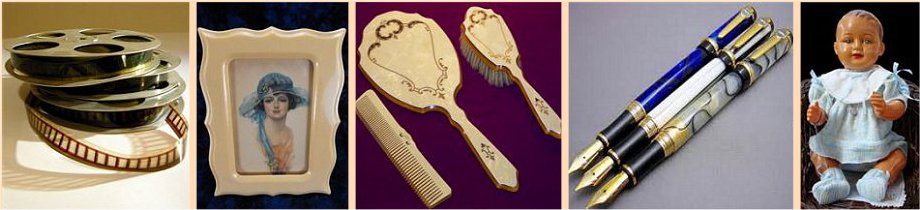
Οι κυριότερες χρήσεις της καμφοράς είναι: ως πλαστικοποιητής (σε αναλογία: 20-30%) σε πλαστικά υλικά από νιτροκυτταρίνη (σελουλόιντ, ζελατίνα) και ως απωθητικό σκώρων και άλλων εντόμων στη φύλαξη και αποθήκευση ενδυμάτων και χαλιών. Καμφορά χρησιμοποιείται ως πλαστικοποιητής σε διάφορα χρώματα και λάκες, αλλά και ως σταθεροποιητικό υλικό σε πυροτεχνήματα πυρίτιδας.
'Εχει διαπιστωθεί ότι η παρουσία καμφοράς σε εργαλειοθήκες προστατεύει τα εργαλεία από την οξείδωση, χάρις στον σχηματισμό από τους ατμούς της ενός λεπτού στρώματος της ουσίας στη μεταλλική επιφάνειά τους. Παλιά και ιστορικώς πολύτιμα κινηματογραφικά φιλμ συντηρούνται καλύτερα παρουσία καμφοράς, η οποία ανακόπτει ή επιβραδύνει την υδρόλυση της οξικής κυτταρίνης από την οποία αποτελούνται. Η φθορά αυτή εκδηλώνεται στους χώρους φύλαξής τους (ταινιοθήκες) από την οσμή οξικού οξέος και αν δεν προληφθεί, μοιραία θα οδηγήσει στην καταστροφή του φιλμ.
 |
 |
 |
|
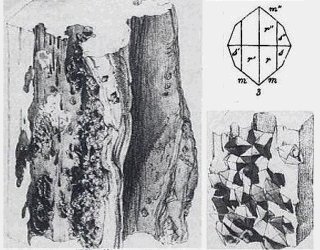
Αριστερά: Στο βιβλίο του Donkin "Dragon's Brain Perfume: An Historical Geography of Camphor" περιγράφεται σχεδόν ό,τι είναι γνωστό σήμερα για την ιστορία της καμφοράς. Κέντρο: Σχέδιο του W. J. Hooker (1852) τομής του δέντρου Dryobalanops aromatica από την οποία "αναβλύζει" καμφορά, η οποία στερεοποιείται σε κρυστάλλους (από το βιβλίο του Donkin, σελ. 41). Δεξιά: Αριστουργηματικά κατασκευασμένη κασέλα φτιαγμένη από ξύλο καμφορόδεντρου. Η αξία του ξύλου αυτού (πέραν από τον αρωματικό χαρακτήρα του) έγκειται στο ότι δεν σαπίζει και ότι ο ρουχισμός που αποθηκεύεται σε κασέλες από ξύλο καμφορόδεντρου, προστατεύεται από τον σκώρο και άλλα έντομα. Επιπλέον, προστατεύει τα διάφορα ασημικά από το μαύρισμα. Κασέλες από ξύλο καμφορόδεντρου όπως η εικονιζόμενη ήταν πανάκριβες και βρίσκονταν μόνο στις κατοικίες υψηλόβαθμων Κινέζων αξιωματούχων και στα αυτοκρατορικά ανάκτορα. |
||

Καμφορά σε διάφορες εμπορικές μορφές της.
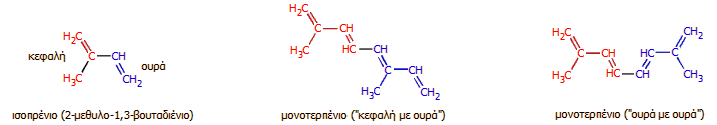
Τερπένια και τερπενοειδή [Αναφ. 2]Σύμφωνα με την IUPAC (International Union of Pure and Applied Chemistry) ορίζονται ως: Τερπένια (terpenes): Οι υδρογονάνθρακες βιολογικής προέλευσης που διαθέτουν σκελετό ανθράκων τυπικά προερχόμενο από το ισοπρένιο [CH2=C(CH3)CH=CH2]. Η τάξη αυτή χωρίζεται σε ημιτερπένια C5, μονοτερπένια C10, σεσκιτερπένια C15, διτερπένια C20, σεστερτερπένια C25, τριτερπένια C30, τετρατερπένια C40 (καροτενοειδή) και πολυτερπένια C5n (το φυσικό καουτσούκ είναι ένα πολυτερπένιο) [Αναφ. 2α]. Τα τερπένια βιοσυντίθενται από μονάδες ισοπρενίου (C5H8) και η βασική μοριακή δομή τους είναι πολλαπλάσιά του, δηλ. (C5H8)n, όπου n είναι ο αριθμός των συνδεδεμένων μεταξύ τους μονάδων ισοπρενίου (κανόνας ισοπρενίου ή κανόνας C5). Οι μονάδας ισοπρενίου μπορεί να συνδέονται μεταξύ τους "κεφαλή με ουρά" ή "ουρά με ουρά" ή να σχηματίζουν δακτυλίους (βλ. παρακάτω: Τερεβινθέλαιο και κύρια συστατικά του).
Η μονάδα ιοσπρενίου μπορεί να θεωρηθεί ως μία από τα πλέον συνηθισμένες δομικές ομάδες φυσικών οργανικών ενώσεων και προέρχονται από μεβαλονικό οξύ (βλ. Χημική ένωση του μήνα: Λυκοπένιο), το οποίο με τη σειρά του προέρχεται από το ακετυλοσυνένζυμο Α. Τερπενοειδή (terpenoids): Φυσικά προϊόντα και σχετικές ενώσεις τυπικά προερχόμενα από μονάδες ισοπρενίου. Περιέχουν οξυγόνο σε διάφορες χαρακτηριστικές ομάδες. Η τάξη αυτή των ενώσεων χωρίζεται σε επιμέρους ομάδες ανάλογα με τον αριθμό ανθράκων με τον ίδιο τρόπο που χωρίζονται τα τερπένια. Ο σκελετός των τερπενοειδών μπορεί να αποκλείνει από την "αυστηρή" προσθετικότητα των μονάδων ισοπρενίου με την απώλεια ή τη μετατόπιση ενός θραύσματος (τυπικά μιας ομάδας μεθυλίου) [Αναφ. 2β]. |
|
Τα φυτά Matricaria parthenium και Chrysanthemum sinensis. Στο πρώτο η καμφορά συναντάται στην αριστερόστροφη μορφή της, ενώ στο δεύτερο στη ρακεμική μορφή. Μια από τις κάπως σπάνιες περιπτώσειςα, όπου μια οπτικώς ενεργή ένωση συναντάται σε διάφορες φυσικές πηγές με τις διαφορετικές μορφές της. |
Χημεία της καμφοράς
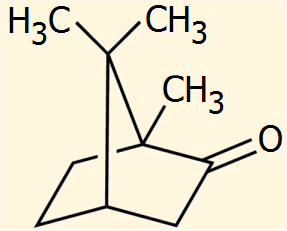
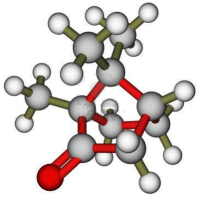
Η καμφορά είναι μια κετόνη, ένα τυπικό τερπενοειδές, δηλ. παράγωγος ένωση ενός τερπενίου και ειδικότερα ενός δικυκλικού μονοτερπενίου. Η καμφορά παρέχει στο σύνολό τους τις τυπικές αντιδράσεις των κετονών.
Η κατά IUPAC ονομασία της καμφοράς είναι 1,7,7-τριμεθυλο-δικυκλο[2.2.1]επταν-2-όνη (βλ. παρακάτω για την ονοματολογία των δικυκλικών ενώσεων). 'Αλλες ημιεμπειρικές ονομασίες της καμφοράς είναι: 2-βορνανόνη, 2-οξο-βορνάνιο, 2-καμφανόνη και 2-κετο-1,7,7-τριμεθυλο-νορκαμφάνιο.
Η καμφορά έχει δύο κέντρα ασυμμετρίας (stereogenic centers) εντοπιζόμενα στους άνθρακες 1 και 4 (βλ. χημικό τύπο παρακάτω). Θεωρητικά θα έπρεπε να έχει 22 = 4 οπτικώς ισομερή, αλλά το σχήμα κλωβού του μορίου δεν επιτρέπει παρά μόνο 2 οπτικώς ισομερή: την (1R,4R)-καμφορά (δεξιόστροφη) και την (1S,4S)-καμφορά (αριστερόστροφη).
|
Αλχημιστικό σύμβολο της καμφοράς (1690). Είναι χαρακτηριστική η παρουσία λεπτομερειών, που σε κάποιο βαθμό συναντώνται στον συντακτικό τύπο της ένωσης. |
Η φυσική καμφορά είναι η δεξιόστροφη (1R,4R)-καμφορά, ενώ η συνθετική καμφορά είναι ρακεμικό μίγμα των δύο. Ωστόσο, στη φύση διαπιστωθεί η παρουσία της αριστερόστροφης (1S,4S)-καμφοράς στο φυτό Matricaria parthenium, όπως και της ρακεμικής μορφής της στο φυτό Chrysanthemum sinensis [Αναφ. 1ζ].
Ο μητρικός υδρογονάνθρακας της καμφοράς (με μεθυλένιο -CH2- στη θέση της καρβονυλικής ομάδας -CO-) είναι το καμφάνιο (ή βορνάνιο), (C10H18, λευκοί κρύσταλλοι, σ.τ. 158-159ºC). Η απομεθυλιωμένη μορφή του καμφανίου είναι το νορκαμφάνιο (ή νορβορνάνιο), (C7H12, λευκοί κρύσταλλοι, σ.τ. 85-88ºC).
[Σημείωση: το πρόθημα νορ- (nor- από το normal) στην ονομασία μιας χημικής ένωσης δηλώνει ότι η δεδομένη ένωση προέκυψε από εκείνη της οποία το όνομα ακολουθεί το πρόθημα, με μείωση του αριθμού ανθράκων μιας αλυσίδας ή ενός δακτυλίου κατά ένα (ή περισσότερων όπως στην περίπτωση του νορκαμφανίου). Το πρόθημα ομο- (homo-, από το homologue) δηλώνει το ακριβώς αντίθετο, δηλ. την αύξηση του αριθμού ανθράκων κατά ένα (βλ. παρακάτω το "ομοκαμφορικό οξύ" σε σχέση με το "καμφορικό οξύ"), περισσότερα εδώ].
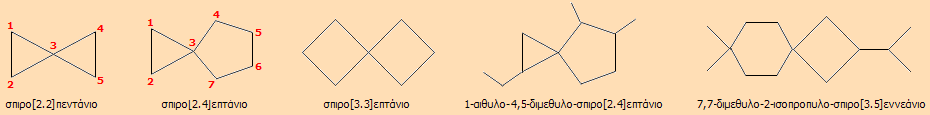
Ονοματολογία δικυκλικών αλκανίων [Αναφ. 3]Τα δικυκλικά αλκάνια είναι κορεσμένοι υδρογονάνθρακες με μόριο που περιλαμβάνει δύο δακτυλίους και με γενικό μοριακό τύπο (αν δεν υπάρχουν άλλες ομάδες) CnH2n-2. Αν οι δακτύλιοι είναι χωρισμένοι μεταξύ τους, τότε δεν υπάρχει πρόβλημα ειδικής ονοματολογίας, αν όμως οι δύο δακτύλιοι έχουν κοινά 1 ή 2 άτομα άνθρακα, τότε για τις ενώσεις αυτές με τους "κολλημένους" δακτυλίους υπάρχει ειδική ονοματολογία. Η ονοματολογία αυτή, που έχει καθιερωθεί από την IUPAC, ακολουθεί απλούς κανόνες και έχει ως εξής:Δικυκλικά αλκάνια με ένα κοινό άτομο άνθρακα. Απλά παραδείγματα αυτών των δικυκλικών αλκανίων είναι τα ακόλουθα:
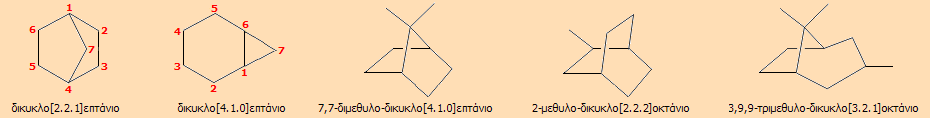
Αν και δεν δείχνεται στους απεικονιζόμενους μοριακούς τύπους, τα δύο επίπεδα που ορίζουν οι δύο δακτύλιοι βρίσκονται σε ορθή γωνία μεταξύ τους (απουσία υποκαταστατών, παρουσία υποκαταστατών μπορεί να υπάρξει απόκλιση). Στις ενώσεις αυτές δίνεται το πρόθημα σπιρο (spiro) ως εκ του τρόπου σύνδεσης μέσω του ενός κοινού ατόμου άνθρακα. Η ρίζα του ονόματος είναι εκείνη του αλκανίου με αριθμό ανθράκων ίσο προς το άθροισμα των ανθράκων και των δύο δακτυλίων. Μεταξύ του προθήματος και της ονομασίας του αντίστοιχου αλκανίου παρεμβάλλονται δυο αγκύλες που περιέχουν τους αριθμούς των μη κοινών ανθράκων του κάθε δακτυλίου χωρισμένους με τελεία. 'Ετσι, η 2η και η 3η εικονιζόμενη ένωση αν και ισομερή σπιροεπτάνια, η 2η είναι το σπιρο[2.4]επτάνιο και η 3η το σπιρο[3.3] επτάνιο. Οι αριθμοί γράφονται κατά αυξανόμενη τιμή ακολουθώντας τη σειρά αρίθμησης των ανθράκων. Η αρίθμηση των ανθράκων ξεκινά από έναν άνθρακα του μικρότερου δακτυλίου αμέσως μετά τον κοινό άνθρακα, περνάει απ' όλο τον δακτύλιο, διέρχεται μέσω του κοινού άνθρακα και συνεχίζει αντίστοιχα στον επόμενο άνθρακα. Στην ονομασία των υποκατεστημένων παραγώγων -εάν υπάρχει επιλογή- χρησιμοποιούνται πάντοτε οι μικρότεροι αριθμοί κάθε δακτυλίου. Δικυκλικά αλκάνια με δύο κοινά άτομα άνθρακα. Απλά παραδείγματα αυτών των δικυκλικών αλκανίων είναι τα ακόλουθα: |
 |
 |
|
Αριστερά: Ο Γερμανός χημικός Julius Bredt (1855-1937). Δεξιά: Ο Φινλανδός χημικός Gustav Komppa (1867 - 1949). Ο πρώτος έδωσε τον σωστό συντακτικό τύπο της καμφοράς και ο δεύτερος τον απέδειξε με την ολική σύνθεση του καμφορικού οξέος. |
|
Προσδιορισμός της χημικής δομής της καμφοράς [Αναφ. 4]. Ο προσδιορισμός της χημικής δομής της καμφοράς απασχόλησε πολλούς χημικούς κυρίως κατά το δεύτερο ήμισυ του 19ου αιώνα. Στην αναζήτηση αυτή συνέβαλαν πολλά γνωστά ονόματα της Χημείας, όπως οι Dumas, Kekulé και ο van't Hoff.
Η ορθή δομή της καμφοράς δημοσιεύτηκε τελικά από τον Γερμανό χημικό Julius Bredt (1855-1937) το 1893, ενώ η ολική σύνθεσή της που απέδειξε τη δομή που πρότεινε ο Bredt, ολοκληρώθηκε από τον Φινλανδό χημικό Gustav Komppa (1867 - 1949) μόλις κατά το 1904. Μέχρι τότε είχαν δημοσιευθεί περίπου 30 διαφορετικοί τύποι.
Στον προσδιορισμό της χημικής δομής της καμφοράς συνέβαλαν πολλά πειραματικά δεδομένα από τα οποία τα κυριότερα ήταν τα εξής:
(α) Ο μοριακός τύπος της καμφοράς ήταν C10H16O. Ο τύπος αυτός είχε προσδιορισθεί σωστά από τον διάσημο Γάλλο χημικό Jean Baptiste André Dumas (1800-1884) ήδη από το 1832.
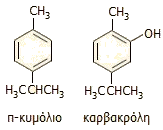
(β) Είχε διαπιστωθεί ότι η καμφορά θερμαινόμενη με P2O5 ή άνυδρο ZnCl2 παρείχε π-κυμόλιο (π-ισοπροπυλο-μεθυλο βενζόλιο), ενώ κατά τη θέρμανσή της με ιώδιο (οξειδωτική αρωματοποίηση) παρείχε καρβακρόλη (5-ισοπροπυλο-2-μεθυλο-φαινόλη, κύριο συστατικό του αιθέριου ελαίου της ρίγανης), γεγονός που συνιστούσε ένδειξη παρουσίας εξαμελούς δακτυλίου άνθρακα. Θα πρέπει να σημειωθεί ότι το κυμόλιο έπαιξε βασικό ρόλο στη χημεία των τερπενίων και των τερπενοειδών και το θεωρούσαν κατά κάποιο τρόπο ως τη μητρική ένωση των τερπενίων. Είναι χαρακτηριστικό το ότι το 1873, ο διάσημος Kekulé (1829-1896) είχε αποδώσει στην καμφορά τον τύπο κετόνης του διυδρογονωμένου κυμολίου.
(γ) 'Ηδη από το 1868 ήταν βέβαιο ότι η καμφορά ήταν μια καρβονυλική ένωση, αφού παρείχε όλες τις σχετικές χαρακτηριστικές αντιδράσεις της καρβονυλομάδας (σχηματισμός οξίμης με υδροξυλαμίνη, υδραζόνες με φαινυλυδραζίνη και παράγωγά της, σεμικαρβαζόνης με σεμικαρβαζίδιο).
 |
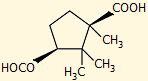
Στερεοχημικός τύπος του φυσικού
καμφορικού οξέος, (1R,3S) |
(δ) Από τα μέχρι τότε δεδομένα ήταν προφανές ότι ο μητρικός υδρογονάνθρακας της καμφοράς είχε τον μοριακό τύπο C10H18 (δηλ. ήταν υδρογονάνθρακας του τύπου CnH2n-2). Το ότι η καμφορά δεν παρείχε αντιδράσεις προσθήκης (π.χ. με Br2) απέκλειε την παρουσία διπλών δεσμών στο μόριό της. Με βάση αυτά προέκυπτε το συμπέρασμα ότι η καμφορά ήταν παράγωγο δικυκλικού και όχι κάποιου ακόρεστου άκυκλου υδρογονάνθρακα.
(ε) Με ήπια οξείδωση με νιτρικό οξύ παρείχε ένα δικαρβοξυλικό οξύ, το καμφορικό οξύ με μοριακό τύπο C10H16O4 ή C8H14(COOH)2 και όχι μονοκαρβονικό οξύ. Το γεγονός αυτό οδηγούσε στο συμπέρασμα ότι η καρβονυλική ομάδα δεν ανήκε σε αλδεϋδική ομάδα (R-CHO), αλλά σε κετο-ομάδα (R-CO-R'), συνεπώς η καμφορά ήταν μια κετόνη και κάπου στο μόριο υπήρχε η ομάδα -CO-CH2-, η οποία κατά την οξείδωσή της άνοιγε παρέχοντας τα δύο καρβοξύλια. Η ευκολία με την οποία το καμφορικό οξύ παρείχε ανυδρίτη αποτελούσε ένδειξη ότι τα δύο καρβοξύλια βρίσκονταν σε θέση cis.
(στ) Κάτω από εντονότερες οξειδωτικές συνθήκες εκτός από το καμφορικό οξύ λαμβανόταν ένα μη κυκλικό κορεσμένο τρικαρβοξυλικό οξύ, το καμφορονικό οξύ με μοριακό τύπο C9H14O6 ή C6H11(COOH)3. Η οξείδωση της καμφοράς σε δύο στάδια παρέχεται από τις ακόλουθες αντιδράσεις:
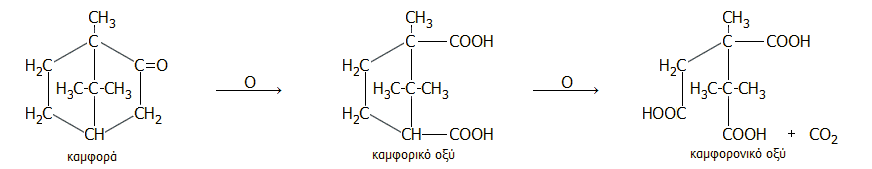
Το 1885, ο Bredt προέβλεψε σωστά τον τύπο του καμφορονικού οξέος με βάση τα προϊόντα της θερμικής διάσπασής του (ισοβουτυρικό οξύ, τριμεθυλοηλεκτρικό οξύ, διοξείδιο του άνθρακα). Με βάση τον τύπο αυτό διατύπωσε την ορθή υπόθεση ότι τα άτομα άνθρακα σε π-θέση του δακτυλίου της καμφοράς γεφυρώνονταν με τη διμεθυλομεθυλενική ομάδα -C(CH3)2-. Η ορθότητα του τύπου του καμφορονικού οξέος επιβεβαιώθηκε 12 χρόνια αργότερα, το 1897 με τη σύνθεσή του από τους Perkin Jr. και Thorpe (J. Chem. Soc., 71:1169, 1897).
Απέμενε μόνο να διευκρινισθεί η θέση του καρβονυλίου ως προς το εξωτερικό μεθύλιο. Το ότι κατά τη θέρμανσή της με ιώδιο (οξειδωτική αρωματοποίηση) η καμφορά παρείχε καρβακρόλη αποτελούσε ισχυρή ένδειξη ότι το καρβονύλιο θα έπρεπε να βρίσκεται προς την πλευρά του εξωτερικού μεθυλίου. Με βάση τα δεδομένα αυτά, το 1893 ο Bredt πρότεινε τον ορθό συντακτικό τύπο της καμφοράς (Ber., 26:3047, 1893).
Αρχικά, η επιστημονική κοινότητα δέχτηκε με αρκετές επιφυλάξεις τον συντακτικό τύπο της καμφοράς που πρότεινε ο Bredt, επειδή βασιζόταν σε "σκόρπιες" πειραματικές ενδείξεις και εικασίες. Ωστόσο, το 1903, ο Φινλανδός χημικός Gustav Komppa πραγματοποίησε τη σύνθεση του καμφορικού οξέος ξεκινώντας με μια συμπύκνωση κατά Claisen των διαιθυλεστέρων του οξαλικού οξέος και του 3,3-διμεθυλογλουταρικού οξέος, αφού προηγήθηκε βέβαια η σύνθεση του τελευταίου με αντίδραση συμπύκνωσης μεσιτυλοξειδίου και μηλονικού διαιθυλεστέρα. Συνοπτικά, τα επιμέρους στάδια της σύνθεσης του καμφορικού οξέος έχουν ως εξής:

Με τη σύνθεση αυτή, o Komppa (Ber., 36:4332, 1903) συμπλήρωσε και ολοκλήρωσε την ολική σύνθεση της καμφοράς, δεδομένου ότι είχε προηγηθεί η "ημισύνθεση" της καμφοράς από τους Haller και Blanc (Compt. rend., 130:376, 1900) από το καμφορικό οξύ, το οποίο όμως είχαν λάβει με οξείδωση της φυσικής καμφοράς. 'Ετσι, δικαιολογημένα, η "τιμή" της πρώτης ολικής σύνθεσης της καμφοράς ανήκει στον Komppa. Η σύνθεση των Haller και Blanc βασίζεται στην ακόλουθη αλληλουχία αντιδράσεων:

H επιτυχής σύνθεση του καμφορικού οξέος από τον Komppa και η εδραιωμένη πλέον σχέση της δομής της καμφοράς με εκείνη της δομής καμφορικού οξέος, κατέστησαν γενικά αποδεκτό και αδιαμφισβήτητο τον συντακτικό τύπο που ο Bredt είχε προτείνει 10 χρόνια νωρίτερα. Η διευκρίνηση της δομής της καμφοράς υπήρξε ένα από πλέον σημαντικά στάδια στην εξέλιξη της χημείας των τερπενίων και των τερπενοειδών.
Βιομηχανική σύνθεση καμφοράς [Αναφ. 5]. Μετά την προηγούμενη πρώτη ολική σύνθεση της καμφοράς (ολική σύνθεση καμφορικού οξέος κατά Komppa + σύνθεση καμφοράς από το καμφορικό οξύ κατά Haller-Blanc) εμφανίστηκαν στη χημική βιβλιογραφία αρκετά απλούστερα σχήματα ολικών συνθέσεων της καμφοράς. Ωστόσο, κανένα σχήμα ολικής σύνθεσης δεν μπορούσε να οδηγήσει σε οικονομικώς συμφέρουσα βιομηχανικής παραγωγή καμφοράς.
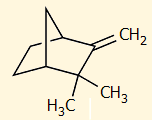
|
Στερεοχημικός τύπος του καμφενίου (2,2-διμεθυλο-3-μεθυλενο-δικυκλο[2.2.1]επτάνιο) |
'Ετσι, η βιομηχανική παραγωγή "τεχνητής" καμφοράς παλαιότερα, αλλά και σήμερα, βασίζεται στο α-πινένιο (α-pinene, pine: πεύκο), ένα τυπικό κυκλικό τερπένιο που διατίθεται σε άφθονες ποσότητες και χαμηλό κόστος, αφού αποτελεί το κύριο συστατικό του τερεβινθελαίου (turpentine), του διαλύτη που είναι ευρύτερα γνωστός ως "νέφτι" και ο οποίος λαμβάνεται με απόσταξη της ρητίνης διαφόρων δέντρων και κυρίως του πεύκου.
Η μέθοδος αυτή αποτελεί την κύρια βιομηχανική οδό παρασκευή ημισυνθετικής καμφοράς και χρησιμοποιήθηκε για πρώτη φορά από τον Komppa, ο οποίος ίδρυσε σχετική βιομηχανία στην πόλη Tainionkoski της Φινλανδίας το 1907. Η τυπική διαδικασία "ημισύνθεσης" καμφοράς από το α-πινένιο, η οποία περιλαμβάνεται σε ελληνικό παλαιό εγχειρίδιο εργαστηριακών ασκήσεων οργανικής σύνθεσης [Αναφ. 5γ]. Περιληπτικά η διαδικασία έχει ως εξής:
Αποστάζεται το τερεβινθέλαιο και συλλέγεται το κλάσμα μεταξύ 154-161ºC, το οποίο αποτελείται σχεδόν από καθαρό α-πινένιο (50-70% του τερεβινθελαίου, ανάλογα με την προέλευσή του). Το λαμβανόμενο α-πινένιο έχει ικανοποιητική καθαρότητα για την περαιτέρω σύνθεση. Ακολουθεί διαβίβαση σ' αυτό υπό ψύξη ξηρού αέριου HCl, οπότε λαμβάνεται βορνυλοχλωρίδιο (αναφέρεται και ως "υδροχλωρικό πινένιο"), ένα στερεό με οσμή καμφοράς. Το βορνυλοχλωρίδιο θερμαίνεται με ισχυρή βάση (π.χ. μίγμα φαινόλης + ΚΟΗ), οπότε αποσπάται ένα μόριο ΗCl και λαμβάνεται το καμφένιο, ένας δικυκλικός υδογονάνθρακας ισομερής προς το α-πινένιο.
Στη συνέχεια, το καμφένιο υπόκειται σε ισχυρώς όξινο περιβάλλον μια τυπική μετάθεση Wagner-Meerwein, οπότε αναδιατάσσονται οι δεσμοί άνθρακα. Η μετάθεση αυτή είναι αντιστρεπτή και χωρεί μέσω σχηματισμού καρβοκατιόντων, τα οποία υφίστανται μόνο σε ισχυρώς όξινο περιβάλλον (βλ. Χημική ένωση του μήνα: Μαγικό οξύ). Το σχηματιζόμενο κατιόν του ισοβορνυλίου "συλλαμβάνεται" από το οξικό οξύ σχηματίζοντας τον εστέρα οξική ισοβορνεόλη, μια αρωματική ουσία η οποία χρησιμοποιείται ευρύτατα σε σαπούνια και διάφορα καλλυντικά.
Ακολουθεί καθαρισμός της οξικής ισοβορνεόλης με απόσταξη υπό ελαττωμένη πίεση και υδρόλυσή της με ισχυρή βάση προς ισοβορνεόλη, δηλ. την αντίστοιχη αλκοόλη, η οποία μπορεί να παραχθεί εύκολα στο εργαστήριο με αναγωγή της καμφοράς (π.χ. με NaBH4). Τελευταίο στάδιο είναι η οξείδωση της ισοβορνεόλης (π.χ. με ΗΝΟ3, KMnO4, NaClO) προς καμφορά, η οποία μπορεί να καθαρισθεί εύκολα με εξάχνωση. Η όλη διαδικασία συνοψίζεται με την ακόλουθη αλληλουχία αντιδράσεων:
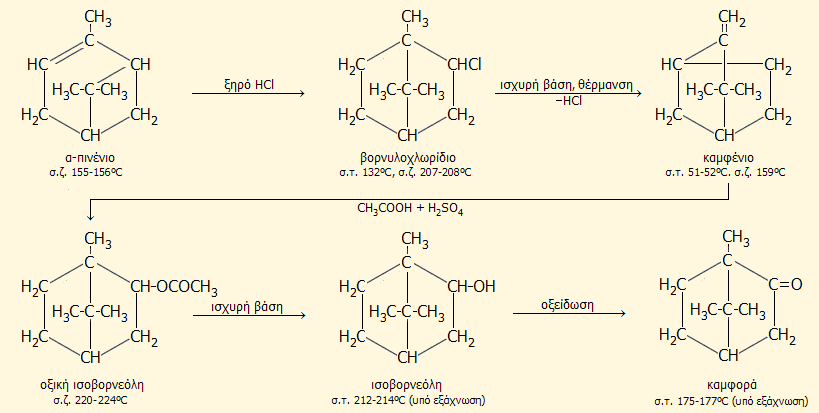
Σε βιομηχανική κλίμακα, η παραπάνω μέθοδος παρουσιάζε σημαντικά προβλήματα ειδικά κατά το πρώτο στάδιο (σύνθεση βορνυλοχλωριδίου) και προτάθηκαν πολλές βελτιώσεις. Σήμερα, η διαδικασία έχει απλουστευθεί, αφού έχει παρακαμφθεί το οχληρό στάδιο σχηματισμού βορνυλοχλωριδίου, με την άμεση καταλυτική μετατροπή του α-πινενίου σε καμφένιο (όξινη κατάλυση) [Αναφ. 6]. Μια σχετικώς πρόσφατη βιομηχανική σύνθεση της καμφοράς βασίζεται πλέον στην ολική σύνθεσή της με πρώτες ύλες πετροχημικά προϊόντα, όπως το βινυλοχλωρίδιο και το κυκλοπενταδιένιο.
Χρήσιμα παράγωγα της καμφοράς. Χρήσιμα παράγωγα της καμφοράς είναι οι αντίστοιχες αλκοόλες βορνεόλη και ισοβορνεόλη (διαστερεομερή). Μεταξύ τους διαφέρουν μόνο ως προς τη θέση του αλκοολικού υδροξυλίου σε σχέση με τη δίεδρο γωνία των δύο δακτυλίων. Στην πρώτη το υδροξύλιο βρίσκεται σε εξω-θέση (exo-position) και στη δεύτερη σε ενδο-θέση (endo-position). Η βορνεόλη κατά κανόνα συνοδεύει την καμφορά στα καμφορούχα φυτά, ενώ η ισοβορνεόλη αποτελεί ένα ενδιάμεσο προϊόν της σύνθεσης καμφοράς. Οι εστέρες των αλκοολών αυτών χρησιμοποιούνται ευρύτατα ως αρωματικές ουσίες σε σαπούνια και διάφορα καλλυντικά κοινής χρήσης.
'Αλλο προϊόν που λαμβάνεται από την καμφορά είναι το καμφορικό οξύ, το οποίο χρησιμοποιείται σε διάφορα αντιιδρωτικά φαρμακευτικά σκευάσματα, έχοντας την ιδιότητα να παραλύει τις νευρικές απολήξεις των ιδρωτοποιών αδένων.
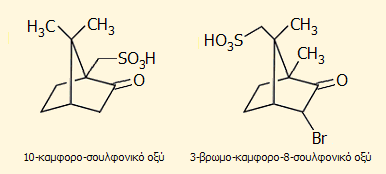
Ιδιαίτερα χρήσιμα στα εργαστήρια χημικής σύνθεσης είναι διάφορα σουλφονικά οξέα (ή άλατά τους) της καμφοράς και βρωμιωμένων παραγώγων τους, όπως το 10-καμφορο-σουλφονικό οξύ και το 3-βρωμο-καμφορο-8-σουλφονικό οξύ. Οι ουσίες αυτές, όπως και αρκετά άλλα παράγωγα της καμφοράς, διατίθενται εμπορικά τόσο στη δεξιόστροφη, όσο και στην αριστερόστροφη μορφή τους και χρησιμοποιούνται ευρύτατα ως χειρόμορφα αντιδραστήρια διαχωρισμού (chiral resolving reagents) σε οπτικούς αντίποδες των ρακεμικών μορφών ενώσεων κατιοντικού τύπου (π.χ. αζωτούχες βάσεις φαρμακευτικής σημασίας), μέσω του σχηματισμού διαστερεομερών αλάτων διαφορετικής διαλυτότητας.
|
|
 |
|
| Βορνεόλη και ισοβορνεόλη: Προϊόντα αναγωγής της καμφοράς, π.χ. με NaBH4. Η αναγωγή της καρβονυλικής ομάδας εισάγει άλλο ένα κέντρο ασυμμετρίας στο μόριο. Οι δύο αλκοόλες είναι μεταξύ τους διαστερεομερείς και ως εκ τούτου διαφέρουν ως προς τις φυσικές ιδιότητες. | Aπό τα πλέον χρησιμοποιούμενα αντιδραστήρια (στη δεξιόστροφη ή στην αριστερόστροφη μορφή τους) για τον διαχωρισμό σε οπτικούς αντίποδες ρακεμικών μορφών οργανικών βάσεων. |