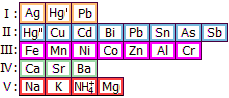 |
Αργίλιο (Al)
|
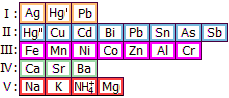 |
Αργίλιο (Al)
|
|
• Mαλακό, ελατό και όλκιμο, αργυρόλευκο μέταλλο, σταθερό ως προς το οξυγόνο και το νερό επικαλυπτόμενο με προστατευτικό στρώμα οξειδίου. Καθίσταται αρκετά σκληρό με προσθήκη σε μικρή αναλογία μετάλλων όπως το Mg και ο Cu. Παρασκευάστηκε από τον H. C. Oersted (Δανία, 1825) με αναγωγή του AlCl3 με μεταλλικό Κ. Η ελληνική ονομασία του προέρχεται από την άργιλο (πυλός), ωστόσο τουλάχιστον ως μέταλλο, στα ελληνικά είναι γνωστότερο ως "αλουμίνιο". Το σύμβολο Al προέρχεται από τη λατινική ονομασία του μετάλλου "aluminium", από τη λέξη "alumen": στυπτηρία, μικτό θειικό άλας K-Al, KAl(SO4)2·12H2O. Στη συνέχεια στυπτηρίες ονομάστηκαν γενικά τα μικτά άλατα με γενικό τύπο MN(SO4)2·12H2O, όπου Μ μονοφορτισμένο κατιόν (κυρίως K+, NH4+) και Ν τριφορτισμένο κατιόν (κυρίως: Al3+, Fe3+, Cr3+). • Η τοξικότητα του μετάλλου και των ανόργανων ενώσεών του θεωρείται μικρή. 'Εχει διαπιστωθεί η συσσώρευσή του στον οργανισμό και πρόσφατες μελέτες δείχνουν κάποια σχέση της συσσωρευμένης ποσότητας Al και της νόσου Altzheimer. • Τα ορυκτά του αργιλίου είναι από τα πλέον άφθονα στη φύση. Αργιλοπυριτικά άλατα του αργιλίου είναι οι διάφοροι γρανίτες [F01]και άστριοι [F02]. Τα ορυκτά αυτά περιέχουν πολλά άλλα ακόμη μέταλλα (K, Na, Fe, Ca, Mg, Ti), αλλά δεν χρησιμοποιούνται για την παραγωγή αργιλίου. Ο βωξίτης, είναι ένα πέτρωμα (μίγμα ορυκτών) που περιέχει διάφορα ορυκτά, ένυδρα οξείδια και υδροξείδια του αργιλίου, όπως διάσπορο (Al2O3·H2O), υδραργιλίτη (Al(OH)3) και οξείδια σιδήρου (Fe2O3) που του δίνουν ένα ανοικτό κοκκινωπό χρώμα [F03] είναι το ορυκτό του αργιλίου από το οποίο αποκλειστικά παράγεται το μέταλλο. Υπάρχει πλήθος ορυκτών του Al τα οποία χρησιμοποιούνται ως έχουν για διάφορους σκοπούς, όπως το κορούνδιο, Al2O3 [F04], ένα από τα σκληρότερα υλικά και του οποίου ερυθρά παραλλαγή (λόγω εμπεριεχομένων ιχνών Cr) είναι ο πολύτιμος λίθος ρουμπίνι [F05]. Ενδιαφέρον παρουσιάζει ένα σπάνιο ορυκτό του αργιλίου, ο κρυόλιθος, Na3AlF6 [F06], που χρησιμοποιείται στη μεταλλουργία του αργιλίου, όπου αναμιγνύεται με την αλουμίνα (Al2O3) για να δημιουργήσει το ευτηκτικό μίγμα που υπόκειται σε ηλεκτρόλυση για την παρασκευή μεταλλικού αργιλίου. • Το 2021 παρήχθησαν παγκοσμίως 68 εκατομ. τόνοι αλουμινίου. Κυριότερες παραγωγοί χώρες: Κίνα, Ρωσία, Καναδάς, ΗΠΑ, Αυστραλία, Βραζιλία, Νορβηγία. • Εφαρμογές: ελαφρά κράματα ευρύτατα χρησιμοποιούμενα στην κατασκευή αυτοκινήτων, αεροπλάνων, οικοδομές, είδη καθημερινής χρήσης (π.χ. μαγειρικά σκεύη, αλουμινόχαρτο, κονσέρβες αναψυκτικών). |
|
F01. Γρανίτης |
F02. 'Αστριος (Na,K)AlSi3O8 |
F03. Βωξίτης, Al2O3·2H2O |
|
F04. Κορούνδιο, Al2O3 |
F05. Ρουμπίνι, Al2O3 |
F06. Κρυόλιθος, Na3AlF6 |
|
Γενικές χημικές ιδιότητες των ενώσεων του Al
Οξειδωτικές καταστάσεις
• Η μόνη σταθερή οξειδωτική κατάσταση του
Al είναι η Al(III).
Διαλυτοποίηση του μετάλλου • Το Al διαλύεται εύκολα σε HCl, με έκλυση H2:
2Al + 6H+
Video 01: Διαλυτοποίηση Al με HCl
• Προσβάλλεται αργά από το αραιό H2SO4, ενώ διαλύεται ταχέως σε πυκνό-θερμό H2SO4:
2Al + 9H2SO4
• Δεν προσβάλλεται από το HNO3, διότι σχηματίζεται επιφανειακό στρώμα Al2O3 που το προστατεύει από περαιτέρω επίδραση του οξέος. • Διαλύεται εύκολα σε διαλύματα ισχυρών βάσεων με έκλυση Η2:
2Al + 2 OH− + 6H2O
Video 02: Διαλυτοποίηση Al με NaOH
Σταθερότητα των διαλυμάτων του • Τα ιόντα Al3+ είναι σταθερά, αλλά είναι απαραίτητη η ελαφριά οξίνιση των διαλυμάτων του για να περιοριστεί η έστω και σε μικρό βαθμό υδρόλυσή τους. • Σε ελαφρώς αλκαλικά (π.χ. αμμωνιακά) διαλύματα σχηματίζεται λευκό, ζελατινώδες (σχεδόν διαφανές) ίζημα Al(OH)3, το οποίο, ως επαμφοτερίζον υδροξείδιο, διαλύεται εύκολα σε περίσσεια ισχυρής βάσης σχηματίζοντας το υδροξυσύμπλοκο [Al(OH)4]−, που βρίσκεται σε ισορροπία με το ανιόν, AlO2− (αργιλικά ανιόντα): Al3+
+ 3 OH−
Al(OH)3 + OH−
[Al(OH)4]−
Σχηματισμός συμπλόκων ιόντων • Τα ιόντα Al3+ σε υδατικά διαλύματα υφίστανται ως άχρωμα εφυδατωμένα σύμπλοκα του τύπου [Al(H2O)6]3+. • Το Al(III) δεν σχηματίζει σύμπλοκα με την NH3 και τα ιόντα CN− (χαρακτηριστική διαφορά από τα ιόντα Zn2+, Ni2+, Co2+). • Σχηματίζει σειρά συμπλόκων με αλογονοϊόντα [AlΧn](3−n)+, από τα οποία τα σταθερότερα είναι εκείνα με ιόντα F−. Επίσης σχηματίζει σύμπλοκα με ιόντα οργανικών οξέων, όπως με τα οξαλικά ιόντα, [Al(C2O4)3]3−.• Σχηματίζει σταθερά σύμπλοκα με ιόντα ΟΗ−, με αποτέλεσμα όλες οι δυσδιάλυτες ενώσεις του να διαλύονται εύκολα σε ισχυρώς αλκαλικά διαλύματα.
Ειδικά χαρακτηριστικά • Δεν σχηματίζει θειούχο άλας με άμεση αντίδραση ιόντων Al3+ και S2− σε υδατικά διαλύματα. Το Al2S3 μπορεί να παρασκευαστεί με θέρμανση Al και S στην προβλεπόμενη στοιχειομετρική αναλογία, υδρολύεται αμέσως μόλις έρθει σε επαφή με το νερό με έκλυση H2S:
Al2S3 + 6H2O
'Ετσι, με επίδραση περίσσειας ιόντων S2− κατά τον διαχωρισμό των κατιόντων της ΙΙΙης ομάδας από τα κατιόντα των άλλων ομάδων, τα ιόντα Al3+ καθιζάνουν ως Al(OH)3 και όχι ως θειούχο άλας (ανάλογη συμπεριφορά παρουσιάζουν και τα ιόντα Cr3+):
Al3+ + 3S2−
+ 3Η2Ο
• Τα ιόντα Al3+ αντιδρούν με 8-υδροξυκινολίνη (QOH) παρέχοντας κίτρινο δυσδιάλυτο ίζημα (η αντίδραση αυτή χρησιμοποιείται και για τον σταθμικό προσδιορισμό Al):
Al3+ + 3QOH
Η αντίδραση πραγματοποιείται παρουσία CH3COONH4 ή ρυθμιστικού διαλύματος NH4Cl - NH3, ώστε να δεσμεύονται τα παραγόμενα ιόντα H+ και να επιτευχθεί ποσοτική καθίζηση των ιόντων Al3+. [V05] • Εάν η καθίζηση του Al(OH)3 πραγματοποιηθεί παρουσία διάφορων οργανικών χρωμάτων, είναι δυνατή η προσρόφηση των μορίων των χρωμάτων στην επιφάνεια του ιζήματος, συνήθως μέσω ηλεκτροστατικών έλξεων. Αποτέλεσμα αυτής της προσρόφησης είναι ο χαρακτηριστικός χρωματισμός του λευκού ή σχεδόν διαφανούς Al(OH)3. Το χρώμα του ιζήματος μπορεί να είναι παραπλήσιο εκείνου του οργανικού χρώματος, όχι όμως κατ’ανάγκη ίδιο. Τα κατά το τρόπο αυτό χρωματισμένα ιζήματα ονομάζονται λάκκες. Χαρακτηριστική ερυθρά λάκκα παρέχει το Al(OH)3 με το οργανικό μόριο αουρινοτρικαρβοξυλικό αμμώνιο, γνωστότερο ως Aluminon:
Al3+ + 3 OH−
+ Aluminon
Τυπικές αντιδράσεις Al3+
1. Ιόντα S2−
Al3+ + 3S2− + 3Η2Ο
2. Iόντα OH−
Al3+ + 3
OH−
Al(OH)3 + OH−
Video 03: Αντίδραση Al3+ με OH−
3. Αμμωνία
Al3+ + 3NH3 + 3Η2Ο
Video 04 : Αντίδραση Al3+ με ΝΗ3
4. 8-υδροξυ-κινολίνη (QOH)
Al3+ + 3QOH
Video 05 : Αντίδραση Al3+ με 8-υδροξυκινολίνη
5. Aluminon Al3+ + 3 OH− + Aluminon
Video 06: Αντίδραση Al3+ με Aluminon
|